Farmeconomia. Health economics and therapeutic pathways 2026; 27(1): 21-33
https://doi.org/10.7175/fe.v27i1.1605
Original research
Analisi costo-conseguenza di differenti strategie di timing di inizio del trattamento con vedolizumab nella malattia di Crohn in Italia
Rossella Bitonti 1, Ilaria Bozzari 1, Eleonora Cerutti 2 , Andrea Marcellusi 3, Agnese Miranda 4, Rita Monterubbianesi 5, Marco Vincenzo Lenti 6, Maria Beatrice Principi 7, Laura Vincenzi 1, Raffaella Viti 8
1 PharmaLex Italy S.p.A., Milan, Italy
2 Clinical Pharmacy Area – Hospital Pharmacy Unit, AO Ordine Mauriziano, Turin, Italy
3 Department of Pharmaceutical Sciences, University of Milan, Milan, Italy
4 A.O.R.N – Vincenzo Monaldi, Naples, Italy
5 Gastroenterology Unit, A.O. “S. Camillo-Forlanini”, Rome, Italy
6 Department of Internal Medicine and Medical Therapy, University of Pavia, Pavia, Italy; Department of Internal Medicine, Fondazione IRCCS Policlinico San Matteo, Pavia, Italy
7 University of Bari Aldo Moro, Bari, Italy
8 Takeda Italia S.p.A., Rome, Italy
Abstract
BACKGROUND: Moderate-to-severe Crohn’s disease (CD) significantly impacts patients and the healthcare system. Timely initiation of biologic therapy is crucial for clinical outcomes and economic efficiency. In Italy, however, many patients eligible for treatment remain on “conventional” drugs, highlighting an undertreatment phenomenon. In this context, this study assessed the clinical and economic impact of early use of vedolizumab compared to delayed management, based on the multicenter LOVE-CD study.
MATERIALS AND METHODS: A cost-consequence model was developed from the perspective of the Italian National Health Service and Italian society. The objective was to compare two therapeutic strategies for CD management: early and late approaches, differing in disease duration and prior anti-TNF exposure. Efficacy data were drawn from the LOVE-CD study, while estimates of direct and indirect costs were derived from the National Tariff and literature. Two scenarios were analyzed: the base case evaluated treatment costs with vedolizumab, including the subsequent phase over 52 weeks; the second scenario, developed with a multidisciplinary panel of Italian experts, included direct costs of the pre-treatment phase, estimating the duration and costs of treatments administered before starting vedolizumab.
RESULTS: The base case analysis showed that the early approach reduces overall costs compared to the late approach in CD management, with a per-patient saving of €6,086 (–10%). The early approach also proved more efficient in terms of cost per responder, both for endoscopic response (–38%) and endoscopic remission (–47%). The scenario analysis extended the evaluation to include the pre-treatment phase: considering these additional costs, the per-patient saving rose to €44,893 (–43%), highlighting even greater economic efficiency for early treatment.
CONCLUSIONS: The results suggested that early initiation of vedolizumab therapy in moderate-to-severe CD can generate significant clinical and economic benefits. These findings support the adoption of more timely and personalized treatment strategies.
Keywords
Crohn’s Disease; Economic analysis; Italy; Biologics; Early; Late
Received: 23 December 2025
Accepted: 17 March 2026
Published: 25 March 2026
Introduzione
La malattia di Crohn (CD) è una patologia infiammatoria cronica dell’intestino, appartenente al gruppo delle malattie infiammatorie croniche intestinali (IBD), che può coinvolgere qualsiasi segmento del tratto gastrointestinale, dalla bocca all’ano. È caratterizzata da un’infiammazione transmurale, persistente e recidivante, che può evolvere in complicanze gravi come stenosi, fistole e ascessi [1]. Il quadro clinico è eterogeneo e dipende dalla localizzazione e dalla severità della malattia. I sintomi più comuni includono diarrea cronica, dolore addominale, sanguinamento rettale, perdita di peso, febbre, artralgie ed eruzioni cutanee [1]. Tali manifestazioni possono compromettere in modo significativo la qualità della vita dei pazienti, limitando la loro capacità di svolgere le attività quotidiane e generando un impatto multidimensionale sul benessere fisico, psicologico e sociale.
Negli ultimi due decenni, la gestione della CD ha beneficiato di significativi progressi terapeutici, in particolare grazie all’introduzione di farmaci avanzati, quali i biologici e le small molecules. Queste nuove terapie hanno ampliato le opzioni di trattamento e stimolato un crescente interesse nella ricerca clinica. Nonostante ciò, il decorso della malattia rimane altamente eterogeneo, rendendo complessa la previsione della risposta individuale alle diverse terapie. Questa variabilità ha favorito l’adozione di un approccio terapeutico personalizzato, finalizzato a modulare le strategie di trattamento in base alle caratteristiche specifiche di ciascun paziente. Tale approccio può prevedere l’impiego di farmaci antinfiammatori, immunosoppressori, agenti biologici e, nei casi più complessi, interventi chirurgici mirati alla gestione delle complicanze [2]. Le terapie avanzate costituiscono un’opzione terapeutica fondamentale nella gestione della CD, in quanto capaci di modificare la storia naturale della patologia e di prevenire la progressione verso forme complicate. Nonostante il loro potenziale, l’impiego dei farmaci biologici nella pratica clinica avviene generalmente in una fase avanzata del percorso terapeutico, a seguito del fallimento di trattamenti convenzionali prolungati, quali corticosteroidi e immunomodulatori. Sebbene tale strategia sia coerente con le raccomandazioni delle principali linee guida [3-7], un utilizzo prolungato di terapie convenzionali può risultare subottimale nei pazienti con malattia attiva e profilo prognostico sfavorevole. Evidenze emergenti suggeriscono che un avvio tempestivo della terapia biologica possa migliorare significativamente gli esiti clinici, ridurre il burden della malattia e prevenire lo sviluppo di complicanze a lungo termine. In particolare, i farmaci biologici hanno dimostrato efficacia nel controllo dell’infiammazione e nell’induzione della remissione clinica, contribuendo a una migliore qualità di vita e a una riduzione delle ospedalizzazioni e degli interventi chirurgici correlati alla malattia [8-11]. La tempistica ottimale per l’inizio della terapia biologica rappresenta ancora un tema controverso nella gestione clinica, condizionata da una molteplicità di fattori, tra cui vincoli regolatori, barriere organizzative e una marcata eterogeneità tra i centri specialistici.
In Italia, evidenze recenti mostrano che circa il 28,6% dei pazienti potenzialmente eleggibili alla terapia biologica continua a essere trattato con farmaci convenzionali, suggerendo un fenomeno di sotto-trattamento in specifici contesti assistenziali [2]. In questo scenario, risulta prioritario approfondire il ruolo del timing nella somministrazione della terapia biologica, al fine di evitare un’esposizione prolungata a terapie convenzionali non più adeguate e di valutare l’impatto clinico ed economico di un intervento tempestivo. Oltre alla tempistica di inizio, anche la scelta del farmaco biologico da impiegare in prima linea rappresenta un determinante cruciale nel percorso terapeutico del paziente e nella sostenibilità del sistema sanitario. Studi condotti nel contesto della rettocolite ulcerosa [12,13] hanno evidenziato come farmaci anti-TNF, pur presentando un profilo di costo-opportunità favorevole nel breve termine, possano risultare meno costo-efficaci rispetto a vedolizumab nel medio-lungo periodo, se si considera l’intero iter terapeutico del paziente.
Questo lavoro si focalizza esclusivamente sul trattamento della CD con vedoluzimab, indicato per il trattamento di pazienti adulti con malattia attiva da moderata a grave, che hanno manifestato una risposta inadeguata, hanno perso la risposta o sono risultati intolleranti alla terapia convenzionale o alla somministrazione di un anti-TNF. Vedolizumab, legandosi in modo specifico all’integrina α4β7, inibisce il reclutamento dei linfociti T nel tratto gastrointestinale, riducendo l’infiammazione intestinale senza compromettere l’immunosorveglianza sistemica e restituendo un profilo di sicurezza favorevole anche in pazienti con comorbidità o rischio di infezioni [14]. La scelta di focalizzarsi su vedolizumab consente pertanto di fornire una valutazione economica coerente e allineata alla pratica clinica nel contesto d’utilizzo di una terapia con un meccanismo d’azione selettivo e differenziato, evidenziato anche nelle linee guida europee [5]. L’assenza di studi clinici condotti su popolazioni comparabili limita la disponibilità di dati solidi e coerenti per un confronto economico diretto tra vedolizumab e le altre terapie disponibili. Tuttavia, in questo contesto, il recente studio multicentrico prospettico LOVE-CD (NCT02646683) [10,11] ha valutato l’efficacia e la sicurezza di vedolizumab in pazienti con CD moderata-severa attiva, stratificati in due coorti in base alla durata della malattia: <24 mesi (early CD) e >24 mesi con precedente esposizione ad anti-TNF (late CD). I risultati hanno mostrato maggiori tassi di remissione clinica e risposta endoscopica nel gruppo trattato precocemente, suggerendo un potenziale beneficio clinico associato a un uso più precoce del farmaco. Alla luce di queste evidenze, il presente studio si propone l’obiettivo di analizzare l’impatto economico e gestionale dell’utilizzo precoce di vedolizumab rispetto alla sua somministrazione tardiva nella CD moderata-severa, adottando la prospettiva del Servizio Sanitario Nazionale (SSN) e della società italiana.
Materiali e metodi
Fonti dei dati
Per la costruzione del modello economico è stata condotta una revisione sistematica della letteratura, finalizzata all’identificazione di analisi economiche rilevanti sul confronto tra approcci terapeutici precoci (early) e tardivi (late) nella gestione della CD. La ricerca è stata effettuata sulla banca dati PubMed, seguendo le linee guida PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses) del 2020 [15]. Sono state utilizzate stringhe specifiche che includevano termini come top-down, step-up, early, late, Crohn, economic e cost, con un filtro temporale di 10 anni. Le parole chiave utilizzate per la ricerca e la strategia di interrogazione sono riportate nella Tabella Supplementare 1. Sono stati selezionati gli articoli pubblicati fino a ottobre 2025, data di chiusura della ricerca bibliografica. Dopo la rimozione dei duplicati, sono stati identificati n = 61 articoli, di cui n = 48 esclusi in fase di screening per motivi metodologici o di pertinenza. Sono stati inclusi n = 13 articoli, a cui si sono aggiunti n = 15 contributi di rilevanza clinica selezionati manualmente da fonti aziendali, per un totale di n = 28 pubblicazioni analizzate (Figura Supplementare 1).
Nella Tabella Supplementare 2 sono elencati gli studi principali utilizzati come fonte dei dati impiegati nell’elaborazione del presente lavoro. Tra questi, lo studio multicentrico prospettico LOVE-CD [10,11] è stato selezionato come principale fonte per i dati di efficacia nella costruzione del modello economico, in virtù di una serie di caratteristiche che lo rendono particolarmente coerente con gli obiettivi del presente lavoro. In primo luogo, si tratta dell’unico studio disponibile che analizza in modo diretto e comparativo un approccio terapeutico early vs late nella CD, fornendo evidenze specifiche sull’impatto della tempistica di inizio della terapia con vedolizumab. Inoltre, la recente pubblicazione dello studio garantisce l’aggiornamento delle evidenze cliniche, assicurando una maggiore aderenza al contesto assistenziale attuale. Infine, il disegno metodologico dello studio, la stratificazione dei pazienti e gli endpoint considerati risultano pienamente allineati con le finalità del progetto. È importante sottolineare che, sebbene gli altri studi emersi dalla revisione della letteratura non siano stati considerati come fonte clinica principale, essi sono stati utilizzati sia nell’elaborazione dell’analisi economica che nella stesura del presente articolo, a supporto delle evidenze emerse.
Struttura del modello
È stato sviluppato un modello costo-conseguenza, basato sulle evidenze dello studio LOVE-CD [10,11], per confrontare due strategie di gestione della CD moderata-severa con vedolizumab: l’approccio precoce (early CD) e quello tardivo (late CD). Le due strategie terapeutiche si distinguono per durata della malattia al momento dell’inizio del trattamento con vedolizumab e per la storia di esposizione ai trattamenti precedenti:
- pazienti con durata di malattia inferiore a 24 mesi (early CD): durata della malattia al basale pari a 30 settimane (range: 7-57) [11];
- pazienti con durata superiore a 24 mesi e precedente esposizione ad anti-TNF (late CD): durata della malattia al basale pari a 582 settimane (range: 313-823) [11].
Al fine di poter individuare i costi diretti e indiretti associati alle differenti strategie terapeutiche in analisi, si è deciso di suddividere il percorso di trattamento dei pazienti in tre fasi distinte, in linea con il protocollo dello studio LOVE-CD [10,11]:
- fase di “Pre-trattamento”: periodo precedente all’inizio della terapia con vedolizumab, caratterizzato dall’impiego di corticosteroidi e immunomodulatori nel gruppo early e, nel gruppo Late, anche di farmaci anti-TNF;
- fase di “Trattamento attivo”: trattamento con vedolizumab della durata di 52 settimane;
- fase di “Consolidamento”: periodo successivo al trattamento attivo, della durata di 52 settimane, in cui viene osservata la risposta clinica ottenuta. In questa fase i pazienti in remissione continuano con vedolizumab, mentre quelli non in remissione passano a una terapia alternativa (es. anti-TNF). La distribuzione dei pazienti tra gli stati di remissione e non-remissione è stata ottenuta dallo studio LOVE-CD [10,11], come descritto nella sezione sui parametri clinici.
In assenza di dati specifici nello studio LOVE-CD [10,11] relativi alla durata delle terapie precedenti l’inizio del trattamento con vedolizumab, la stima temporale della fase di pre-trattamento è stata definita tramite consultazione con un panel multidisciplinare composto da gastroenterologi, farmacisti ospedalieri e farmacoeconomisti. In accordo con la pratica clinica italiana, per i pazienti late CD è stata considerata una fase di “Pre-trattamento” più estesa (52 settimane vs 104 settimane; Tabella Supplementare 3), coerente con una diagnosi superiore ai 24 mesi e con l’esposizione anche a precedenti trattamenti con anti-TNF. Al contrario, per i pazienti early CD è stata considerata una durata più breve, coerente con una diagnosi <24 mesi e limitata all’impiego di terapie convenzionali. Le fasi successive, ovvero il “Trattamento attivo” con vedolizumab e il “Consolidamento”, sono state stimate coerentemente con i risultati del LOVE CD pari a una durata pari di 52 settimane ciascuna, in linea con il follow-up clinico riportato nello studio [10,11] (Figura 1).
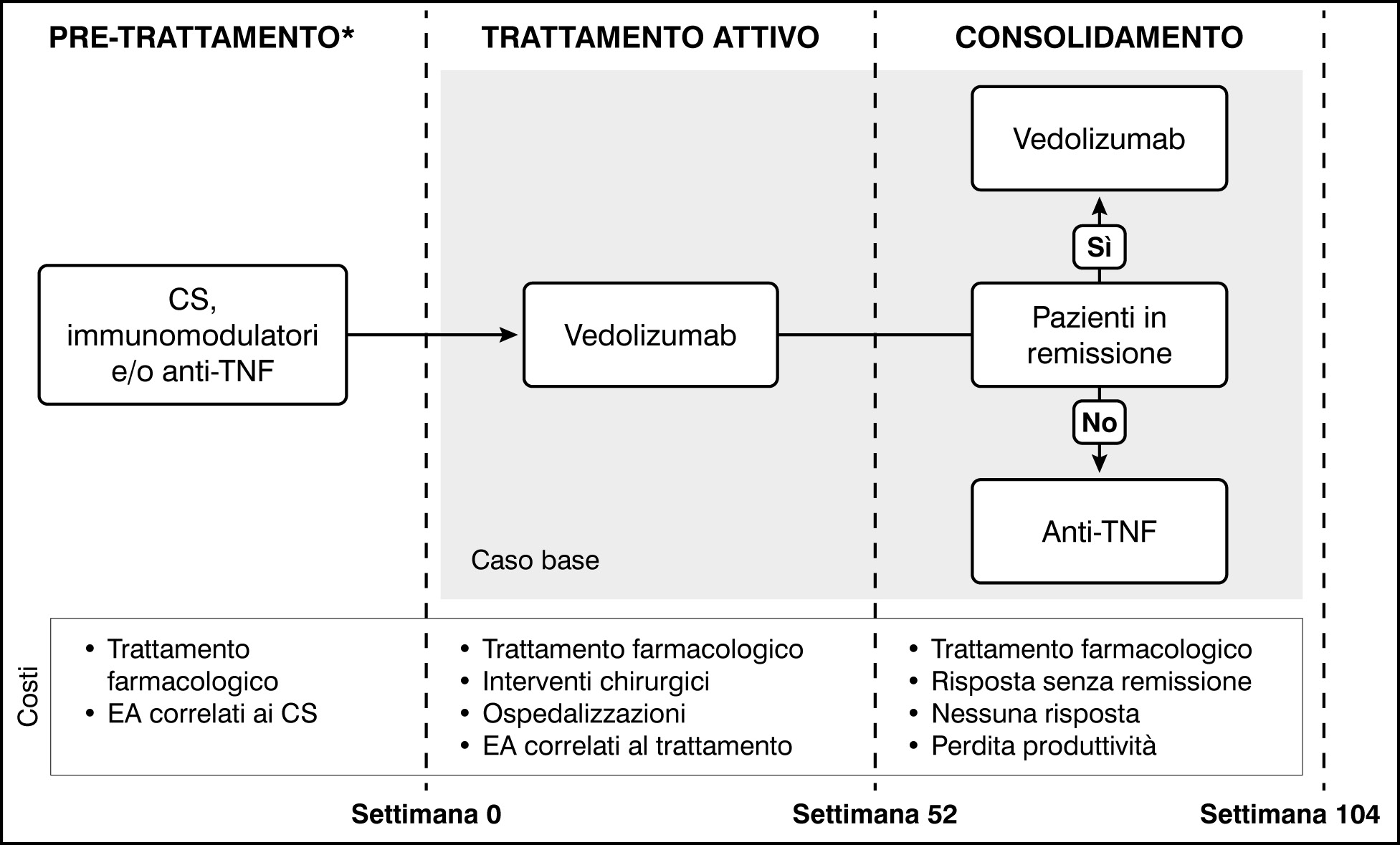
Figura 1. Struttura del modello
*Fase di durata differente tra i due bracci di trattamento (early CD: 52 settimane; late CD: 104 settimane); non considerata nel caso base, ma inclusa nell’analisi di scenario.
CS: corticosteroidi; EA: eventi avversi; TNF: fattore di necrosi tumorale
Analisi per scenari e orizzonte temporale
Il modello presenta i risultati attraverso due scenari distinti.
- Caso base: esclude la fase di “Pre-trattamento” per garantire la comparabilità della durata del follow-up tra i gruppi e isolare i benefici clinici ed economici attribuibili esclusivamente al trattamento con vedolizumab. Il confronto riguarda 52 settimane di “Trattamento Attivo” con vedolizumab seguite da 52 settimane di “Consolidamento”. In questo scenario, sono considerati solo i costi del trattamento farmacologico, degli interventi chirurgici, delle ospedalizzazioni, degli eventi avversi legati al trattamento, delle risposte senza remissione e della perdita di produttività. I risultati sono ottenuti esclusivamente dai dati dello studio LOVE-CD, rendendo questo scenario più robusto e meno soggetto a incertezze modellistiche.
- Scenario alternativo: include la fase di “Pre-trattamento” per entrambe le strategie, pur essendo di diversa durata (early CD: 52 settimane; late CD: 104 settimane). Questo approccio permette di valutare anche l’impatto clinico ed economico delle fasi precedenti l’inizio del trattamento con vedolizumab, offrendo una visione più completa del percorso assistenziale e del carico economico complessivo per il paziente. Oltre ai costi del caso base, vengono inclusi anche i costi delle terapie farmacologiche precedenti e degli eventi avversi legati ai corticosteroidi. Anche se offre una visione più completa del percorso del paziente, questo scenario è meno robusto del caso base, perchè necessita di assunzioni relative alla durata del trattamento con corticosteroidi e delle terapie farmacologiche precedenti. Tali assunzioni sono state definite in collaborazione con un panel di esperti italiani. Tutti gli outcome sono espressi come costo totale per paziente e costo per paziente responder (clinico ed endoscopico).
Popolazione del modello
Il profilo dei pazienti considerati nel modello riflette le caratteristiche della popolazione arruolata nello studio LOVE-CD [10,11], ovvero soggetti adulti, di età compresa tra 18 e 80 anni, affetti da CD attiva moderata-severa, con un indice Crohn’s Disease Activity Index (CDAI) compreso tra 220 e 450 e presenza documentata di ulcere durante l’endoscopia. I pazienti sono stati suddivisi in due coorti distinte, al fine di rappresentare in modo realistico i differenti percorsi terapeutici osservati nella pratica clinica. La prima coorte comprende individui con diagnosi di CD da meno di due anni, naïve al trattamento con farmaci biologici e trattati esclusivamente con corticosteroidi e/o immunomodulatori (early CD). La seconda coorte include pazienti con diagnosi da oltre due anni, già sottoposti a trattamenti con corticosteroidi, immunomodulatori e almeno un agente anti-TNF (late CD). Tale distinzione consente di rappresentare in maniera differenziata le implicazioni cliniche ed economiche associate a ciascun approccio terapeutico, in linea con gli obiettivi del presente studio.
Parametri clinici
I dati di efficacia utilizzati nel modello derivano dallo studio clinico multicentrico LOVE-CD, che ha valutato l’efficacia e la sicurezza di vedolizumab in pazienti adulti affetti da CD attiva moderata-severa [10,11]. L’endpoint primario dello studio era rappresentato dalla proporzione di pazienti in remissione clinica ed endoscopica, definita come CDAI ≤150 e Crohn’s Disease Simple Endoscopic Score (SES-CD) <4, valutata sia alla settimana 26 che alla settimana 52. Per quanto concerne la fase di “Pre-trattamento”, considerata nell’analisi di scenario, lo studio ha fornito informazioni qualitative sulle terapie impiegate prima dell’introduzione di vedolizumab (corticosteroidi, immunomodulatori, anti-TNF), senza tuttavia riportare dati quantitativi sulla durata di ciascun trattamento. Per colmare questa lacuna, la stima della durata della fase di “Pre-trattamento” è stata definita attraverso una consultazione strutturata con un panel multidisciplinare di esperti clinici, composto da gastroenterologi, farmacisti ospedalieri e farmacoeconomisti, sulla base della pratica clinica italiana. In particolare, è stato ipotizzato che i pazienti classificati come early CD ricevano corticosteroidi per una durata di 13 settimane e immunomodulatori per 52 settimane, mentre i pazienti late CD presentino un percorso terapeutico più articolato, con una durata di 26 settimane per la terapia corticosteroidea, 52 settimane di trattamento con immunomodulatori e un’aggiunta di 78 settimane di esposizione ad anti-TNF. Questa differenziazione temporale riflette le diverse strategie terapeutiche adottate nella pratica clinica italiana e consente di rappresentare in modo più accurato le implicazioni economiche e cliniche associate a ciascun gruppo. I dettagli relativi a questa fase sono riportati in Tabella Supplementare 3.
I tassi di risposta e remissione endoscopica osservati nello studio LOVE-CD, riferiti alla popolazione intention-to-treat (ITT), sono stati utilizzati per stimare la distribuzione dei pazienti nelle diverse fasi del percorso terapeutico [10,11]. In particolare, la proporzione di pazienti che proseguono il trattamento con vedolizumab nella fase “Consolidamento” è stata determinata sulla base della percentuale di pazienti in remissione endoscopica alla settimana 52 (Tabella I) [10,11]. I tassi di risposta endoscopica sono stati invece utilizzati per identificare i pazienti che, pur non raggiungendo la remissione, hanno ottenuto una risposta al trattamento. La quota di pazienti responder non in remissione è stata calcolata come differenza tra il tasso di risposta endoscopica e quello di remissione, mentre la restante proporzione è stata classificata come non responder.
Oltre ai tassi di risposta e remissione, il modello ha integrato ulteriori parametri clinici finalizzati alla stima dell’utilizzo di risorse sanitarie associate agli esiti del trattamento, inclusi i tassi di ospedalizzazione e di intervento chirurgico, e l’incidenza di eventi avversi correlati al trattamento con vedolizumab e eventi avversi correlati all’utilizzo di corticosteroidi, differenziata tra i gruppi early e late CD in base alle evidenze disponibili e alla pratica clinica corrente [10,11]. I dati clinici impiegati nell’analisi, sia per il caso base sia per l’analisi di scenario, sono presentati nella Tabella I.
|
Parametro |
Early CD |
Late CD |
|---|---|---|
|
Proporzione di pazienti in remissione endoscopica alla settimana 52 (%) |
51,2 |
27,0 |
|
Proporzione di pazienti in risposta endoscopica alla settimana 52 (%) |
57,0 |
35,6 |
|
Proporzione pazienti che richiedono una chirurgia (%) |
0,0 |
4,6 |
|
Proporzione pazienti che richiedono una ospedalizzazione (%) |
3,5 |
26,4 |
|
Proporzione di pazienti con eventi avversi seri correlati al trattamento con vedolizumab* (%) |
2,4 |
16,6 |
|
Proporzione di pazienti con eventi avversi correlati ai corticosteroidi** (%) |
35,0 |
29,0 |
|
Proporzione di pazienti con risposta senza remissione (%) |
5,8 |
8,6 |
|
Proporzione pazienti senza risposta endoscopica (%) |
43,0 |
64,4 |
Tabella I. Parametri clinici utilizzati nel modello [10,11]
*Sono stati considerati gli eventi avversi seri con una frequenza ≥1,5%
**Percentuale di pazienti che assume corticosteroidi nella fase di “Pre-trattamento”, considerato nello scenario alternativo
CD: malattia di Crohn
Parametri economici
Coerentemente con la prospettiva adottata, nel caso base sono stati considerati sia i costi diretti a carico del SSN, includendo sia i costi farmacologici sia quelli associati all’impiego di altre risorse sanitarie, che i costi indiretti derivanti dalla perdita di produttività.
Costo del trattamento farmacologico
I costi farmacologici sono stati stimati per ciascuna fase del percorso terapeutico – “Pre-trattamento”, “Trattamento attivo” e “Consolidamento” – sulla base dei dosaggi e delle frequenze di somministrazione riportati nei rispettivi Riassunti delle Caratteristiche del Prodotto (RCP), distinguendo tra fase di induzione e fase di mantenimento (Tabella Supplementare 4). I prezzi per confezione dei farmaci sono stati considerati al netto delle riduzioni di legge (5% + 5%) (Tabella II) e ricavati dalle liste dei farmaci in classe A e H dell’Agenzia Italiana del Farmaco (AIFA) [16]. Per i farmaci per i quali sono disponibili formulazioni biosimilari, è stato adottato un valore medio tra il prezzo del prodotto originator e quello del biosimilare, al fine di riflettere in modo più realistico le condizioni di acquisto nella pratica ospedaliera. Le durate dei trattamenti farmacologici sono dettagliate nel paragrafo Parametri clinici.
|
Nome farmaco |
Contenuto confezione |
Prezzo per confezione (€) |
Fonte |
|
Prednisone |
20 compresse |
1,36 |
AIFA [16] |
|
Azatioprina |
50 compresse |
7,13 |
|
|
Infliximab |
1 flacone |
424,91 |
|
|
Adalimumab |
2 penne preriempite |
806,86 |
|
|
Vedolizumab |
1 flacone |
2.036,04 |
Tabella II. Prezzi a confezione dei trattamenti farmacologici inclusi nell’analisi
Costo degli eventi avversi associati all’utilizzo di corticosteroidi
Per quanto riguarda gli eventi avversi associati all’uso di corticosteroidi, i costi sono stati imputati in funzione della proporzione di pazienti trattati con questa classe farmacologica nella fase di “Pre-trattamento” nei due scenari analizzati, come riportato in Tabella I. I costi totali sono stati calcolati sulla base delle frequenze specifiche di ciascun evento e dei relativi costi unitari di trattamento, riportati in Tabella Supplementare 5. Le frequenze degli eventi avversi sono state differenziate tra i due approcci terapeutici in funzione della durata dell’esposizione ai corticosteroidi, secondo quanto indicato dallo studio di riferimento (Colombo et al., 2023 [17]) e validato dal panel di esperti clinici coinvolti. In particolare, è stato assunto che i pazienti trattati secondo l’approccio early CD presentino una frequenza di eventi avversi associata a un’esposizione inferiore a 3 mesi, mentre per i pazienti late CD l’esposizione sia superiore a 6 mesi. Tra gli eventi considerati nell’analisi figurano insonnia, disturbi dell’umore, ipertensione, diabete e osteoporosi, ciascuno caratterizzato da un impatto economico distinto in funzione della durata del trattamento corticosteroideo.
Costo delle ospedalizzazioni e degli interventi chirurgici
Sono stati inclusi i costi associati all’ospedalizzazione e agli interventi chirurgici, stimati sulla base dei tassi di incidenza anticipati in Tabella I, in combinazione con i relativi costi unitari (Tabella III).
|
Costi unitari (€) |
Fonti |
||
|---|---|---|---|
|
Early CD |
Late CD |
||
|
Interventi chirurgici |
5.885 |
Media tariffe DRG 149, 152, 153 [18] |
|
|
Ospedalizzazioni |
3.236 |
Tariffa DRG 179 [18] |
|
|
EA correlati al trattamento con vedolizumab |
4.050 |
Media pesata tariffe DRG 172, 173, 179, 180, 181,464, 576 [18] |
|
|
Risposta senza remissione |
439 |
[13] |
|
|
Nessuna risposta |
14.128 |
[13] |
|
Tabella III. Costi unitari altre risorse sanitarie
CD: malattia di Crohn; EA: eventi avversi
Costo degli eventi avversi correlati al trattamento con vedolizumab
I costi associati alla gestione degli eventi avversi correlati al trattamento con vedolizumab sono stati stimati considerando le percentuali di incidenza specifiche per ciascun approccio terapeutico (early e late CD), derivate dallo studio LOVE-CD e riportate in Tabella I, in combinazione con il costo unitario per evento [10,11]. Quest’ultimo è stato calcolato come media delle tariffe associate ai DRG 172-173 – Neoplasie maligne dell’apparato digerente con e senza CC, DRG 179 – Malattie infiammatorie dell’intestino, DRG 180-181 – Occlusione gastrointestinale con e senza CC, DRG 464 – Segni e sintomi senza CC, DRG 576 – Setticemia senza ventilazione meccanica ≥96 ore, età >17 anni [18], pesata per le rispettive incidenze riportate nello studio LOVE-CD (Tabella III) [10,11].
Costi associati alle risposte cliniche parziali o assenti
La stima dei costi associati alle risposte cliniche parziali o assenti è stata effettuata sulla base della proporzione di pazienti che hanno ottenuto una risposta endoscopica senza raggiungere la remissione, oppure che non hanno risposto al trattamento, come riportato in Tabella III. Per i pazienti senza risposta, è stato ipotizzato un passaggio al trattamento con infliximab [13], in linea con la pratica clinica osservata nei pazienti con risposta subottimale alla terapia con vedolizumab. I costi associati a tale switch terapeutico sono stati calcolati tenendo conto della durata e del regime di somministrazione previsti per infliximab (Tabella III). Il costo associato alla risposta senza remissione è stato derivato sulla base delle evidenze disponibili in letteratura (Tabella III) [13].
Costi indiretti (perdita produttività)
Nel caso base, è stata considerata anche una prospettiva estesa che include i costi indiretti legati alla perdita di produttività, al fine di valutare l’impatto socio-economico complessivo della CD oltre ai soli costi sanitari diretti. I costi indiretti sono stati stimati tenendo conto di tre componenti principali: assenteismo, presenteismo e assistenza informale. La quantificazione è stata effettuata utilizzando il costo orario medio del lavoro in Italia (€30,9/ora), come riportato da Eurostat, e il numero medio di ore lavorative settimanali (40 ore) [19]. Le riduzioni dell’attività lavorativa sono state differenziate tra pazienti in remissione e pazienti con malattia attiva, sulla base delle evidenze pubblicate da Holko et al. (2023) [20], che riportano una riduzione della produttività pari al 25% in fase di remissione e al 55% in fase attiva. In assenza di dati specifici, è stato possibile calcolare i costi indiretti esclusivamente per la fase di “Consolidamento”, in quanto rappresentativa di un miglioramento clinico con potenziale ritorno parziale alla produttività.
Risultati
Caso base
L’analisi di caso base ha evidenziato una differenza significativa nei costi complessivi tra la strategia early e late nella gestione della CD. Il costo totale per paziente nell’approccio precoce è stato pari a €56.380, mentre per l’approccio tardivo è stato di €62.466, pari a una riduzione assoluta di €6.086 (-10%) (Tabella IV).
La valutazione disaggregata delle risorse sanitarie ha mostrato che la strategia precoce è associata a una riduzione sostanziale dei costi per ospedalizzazioni (-87%) e per interventi chirurgici (-100%), rispetto all’approccio tardivo. Questi dati sottolineano come il trattamento precoce con vedolizumab sia associato a una minore necessità di ricorso a ospedalizzazione e chirurgia durante il periodo considerato. Ulteriori riduzioni sono state osservate nei costi per eventi avversi correlati al trattamento (-86%) e nei costi riferiti ai pazienti senza risposta clinica (-33%). Sebbene i costi farmacologici della fase di consolidamento siano stati superiori nell’approccio precoce (€6.776 vs €3.573), in linea con una maggiore efficacia clinica, il risparmio complessivo ottenuto nelle risorse sanitarie più rilevanti (ospedalizzazioni, chirurgia, eventi avversi e pazienti senza risposta) compensa ampiamente questa differenza, determinando una riduzione netta dei costi totali per paziente. Inoltre, la perdita di produttività si è ridotta di €4.666€ (-15%).
Questo risultato è stato confermato dall’analisi del costo per paziente responder: con l’approccio precoce, il costo per ogni paziente che ottiene risposta endoscopica è sceso nel trattamento tardivo (-38%), mentre per la remissione endoscopica il costo si è ridotto del -47%. Questo indica una maggiore efficienza economica dell’approccio precoce, in termini di costo per beneficio clinico raggiunto.
Nella Tabella IV è possibile osservare la sintesi dettagliata degli output economici per ciascuna voce di costo inclusa nell’analisi del caso base.
|
(A) Early CD |
(B) Late CD |
Δ – A vs B (€) |
Δ – A vs B (%) |
||
|
Costi diretti (€) |
Costi farmacologici |
||||
|
17.815 |
17.815 |
0 |
0% |
|
|
6.776 |
3.573 |
3.203 |
90% |
|
|
24.591 |
21.389 |
3.203 |
15% |
|
|
Costi risorse sanitarie |
|||||
|
0 |
271 |
-271 |
-100% |
|
|
113 |
854 |
-741 |
-87% |
|
|
97 |
672 |
-575 |
-86% |
|
|
25 |
38 |
-12 |
-33% |
|
|
6.075 |
9.099 |
-3.023 |
-33% |
|
|
6.311 |
10.934 |
4.623 |
-42% |
|
|
Costi diretti totali |
30.902 |
32.322 |
-1.420 |
-4% |
|
|
Costi indiretti (€) |
Perdita di produttività |
25.477 |
30.144 |
-4.666 |
-15% |
|
Costi indiretti totali |
25.477 |
30.144 |
-4.666 |
-15% |
|
|
Costi totali |
56.380 |
62.466 |
-6.086 |
-10% |
|
|
Costo per responder (€) |
Risposta endoscopica* |
98.912 |
158.370 |
-59.458 |
-38% |
|
Remissione endoscopica** |
110.117 |
208.814 |
-98.697 |
-47% |
|
Tabella IV. Sintesi degli output economici del caso base – prospettiva SSN e sociale
*Calcolato come il costo totale diviso per il tasso di risposta endoscopica (early CD: 57,0%, late CD: 35,6%), **Calcolato come il costo totale diviso per il tasso di remissione endoscopica (early CD: 51,2%, late CD: 27,0%)
EA: eventi avversi; CD: malattia di Crohn
Analisi di scenario
Nell’analisi di scenario (prospettiva SSN e Sociale), oltre ai costi inclusi nel caso base, sono stati inclusi i costi associati alla fase di “Pre-trattamento”, ovvero i costi del trattamento farmacologico e degli eventi avversi correlati all’utilizzo dei corticosteroidi, per rappresentare in modo più completo l’assorbimento di risorse sanitarie nella gestione della CD.
L’inclusione di tali voci ha ampliato significativamente la differenza complessiva tra le due strategie terapeutiche. In questo scenario, il costo totale per paziente è risultato pari a €58.521 per l’approccio precoce e €103.414 per quello tardivo (-43%) (Tabella V).
Nei pazienti trattati precocemente, il costo del pre-trattamento farmacologico è risultato pari a €1.354, mentre nell’approccio tardivo di €40.206 (-97%). Questo dato evidenzia come l’inizio tempestivo della terapia riduca drasticamente il ricorso e la durata al pre-trattamento farmacologico. Le altre componenti di costo si sono confermate invariate, con l’approccio precoce associato a una riduzione della spesa nella maggior parte delle risorse sanitarie analizzate, con differenze particolarmente rilevanti per il totale dei costi diretti e per i costi indiretti legati alla perdita di produttività (Tabella V).
|
(A) Early CD |
(B) Late CD |
Δ – A vs B (€) |
Δ – A vs B (%) |
||
|---|---|---|---|---|---|
|
Costi diretti (€) |
Costi farmacologici |
||||
|
1.354 |
40.206 |
-39.851 |
-97% |
|
|
17.815 |
17.815 |
0 |
0% |
|
|
6.776 |
3.573 |
3.203 |
90% |
|
|
25.945 |
61.594 |
-35.649 |
-58% |
|
|
Costi risorse sanitarie |
|||||
|
0 |
271 |
-271 |
-100% |
|
|
113 |
854 |
-741 |
-87% |
|
|
97 |
672 |
-575 |
-86% |
|
|
787 |
743 |
45 |
6% |
|
|
25 |
38 |
-12 |
-33% |
|
|
6.075 |
9.099 |
-3.023 |
-33% |
|
|
7.098 |
11.676 |
-4.578 |
-39% |
|
|
Costi diretti totali |
33.044 |
73.270 |
-40.227 |
-55% |
|
|
Costi indiretti (€) |
Perdita di produttività |
25.477 |
30.144 |
-4.666 |
-15% |
|
Costi indiretti totali |
25.477 |
30.144 |
-4.666 |
-15% |
|
|
Costi totali |
58.521 |
103.414 |
-44.893 |
-43% |
|
|
Costo per responder (€) |
Risposta endoscopica* |
102.669 |
164.386 |
-61.717 |
-38% |
|
Remissione endoscopica** |
114.299 |
216.745 |
-102.446 |
-47% |
|
Tabella V. Sintesi degli output economici dello scenario alternativo – prospettiva SSN e sociale
*Calcolato come il costo totale diviso per il tasso di risposta endoscopica (early CD: 57,0%; late CD: 35,6%), **Calcolato come il costo totale diviso per il tasso di remissione endoscopica (early CD: 51,2%; late CD: 27,0%)
EA: eventi avversi; CD: malattia di Crohn
Discussione
I risultati dell’analisi condotta evidenziano come l’impiego precoce di vedolizumab nella gestione della CD moderata-severa sia associato a una maggiore efficienza economica rispetto all’approccio tardivo, sia nel caso base sia nelle analisi di scenario. Questo risultato è particolarmente rilevante in un contesto di crescente pressione sui budget sanitari, dove l’ottimizzazione delle risorse rappresenta una priorità strategica. Il risparmio osservato può essere attribuito a diversi fattori, tra cui una maggiore probabilità di raggiungere la remissione endoscopica nei pazienti trattati precocemente, una minore incidenza di eventi clinici avversi e una ridotta necessità di ricorrere a terapie alternative più costose in caso di risposta subottimale. Inoltre, l’inclusione dei costi indiretti ha ulteriormente rafforzato il vantaggio dell’approccio precoce, evidenziando benefici anche in termini di produttività lavorativa e riduzione del carico assistenziale informale. Un dato particolarmente rilevante, emerso da recenti analisi italiane [21], è che circa il 28,6% dei pazienti potenzialmente eleggibili alla terapia biologica continua a essere trattato con farmaci convenzionali. Questo fenomeno di sotto-trattamento potrebbe riflettere barriere organizzative, vincoli regolatori o disomogeneità tra centri specialistici e strutture periferiche. Tale gap terapeutico rappresenta un’importante opportunità di miglioramento, sia in termini di equità di accesso alle terapie avanzate, sia di efficienza complessiva del sistema. La capacità di identificare precocemente i pazienti che potrebbero beneficiare maggiormente di un trattamento biologico consente, infatti, di personalizzare l’intervento terapeutico, migliorando gli esiti clinici e riducendo i costi sanitari associati a complicanze, ospedalizzazioni e progressione della malattia.
I risultati della presente analisi confermano l’idea consolidata che un intervento precoce con farmaci efficaci sia altamente vantaggioso nella CD, sebbene le evidenze disponibili finora si basino principalmente su pazienti trattati con agenti anti-TNF. Il concetto è stato inizialmente esplorato con infliximab nello studio step-up/top-down [11], replicato nella popolazione pediatrica [22] e infine confermato nello studio PROFILE [8]. Il trial REACT [9] ha dimostrato che un approccio proattivo e precoce nella gestione della CD è associato a una riduzione significativa del rischio di ospedalizzazione e interventi chirurgici. Inoltre, lo studio di Marchetti et al. (2013) [23], ha evidenziato la costo-efficacia della strategia top-down nei pazienti con malattia luminale, mentre [17] Colombo et al. (2023) [17], hanno sottolineato l’impatto economico negativo dell’uso prolungato di corticosteroidi. Inoltre, il già citato studio di Degli Esposti et al. (2023) [21], ha documentato una persistente tendenza al sottoutilizzo dei biologici, rafforzando la necessità di interventi sistemici per migliorare l’appropriatezza prescrittiva. Le evidenze dei trial citati suggeriscono che l’elevata efficacia dell’intervento biologico precoce non è legata al tipo di trattamento, ma al momento della sua introduzione [11]. Infatti, tassi di remissione più elevati sono stati osservati anche con altri biologici, come guselkumab o ustekinumab, quando il trattamento è iniziato nelle fasi iniziali della malattia [24,25]. Considerando che alcuni anti-TNF, come infliximab, vengono solitamente prescritti in combinazione con immunomodulatori, mentre vedolizumab è generalmente somministrato in monoterapia, quest’ultimo potrebbe essere preferibile come agente avanzato di prima linea, almeno nei pazienti con sintomi intestinali isolati (cioè senza manifestazioni extraintestinali o malattia perianale) [11]. Difatti, la perdita di efficacia di vedolizumab è molto più frequente quando somministrato dopo agenti anti-TNF, rispetto a quando viene utilizzato come primo trattamento, riservando gli anti-TNF ai pazienti refrattari o con manifestazioni extraintestinali [11]. È importante sottolineare che la definizione di malattia precoce è in continua evoluzione. Nel primo studio top-down, è stato utilizzato un limite di 4 anni per definirla. Successivamente, il parere degli esperti ha suggerito un limite di 18 mesi, mentre il più recente studio PROFILE ha adottato un cut-off di 6 mesi. Data l’assenza di una raccomandazione uniforme e il fatto che molti pazienti presentano una fase preclinica della malattia mesi o anni prima della diagnosi, la presente analisi ha considerato la definizione di malattia CD precoce come quella diagnosticata da meno di 2 anni e non trattata con terapie avanzate (naïve o trattata solo con corticosteroidi e/o immunomodulatori), in linea con lo studio LOVE-CD [11]. Il presente studio si distingue da altri modelli economici in ambito gastroenterologico per il focus sulla finestra temporale di posizionamento del trattamento biologico, piuttosto che sul sequenziamento terapeutico [12]. Tale approccio consente di esplorare una dimensione ancora poco indagata, ma potenzialmente decisiva per migliorare gli esiti clinici e la sostenibilità del sistema. Questo studio apporta un contributo originale ed è la prima analisi di costo conseguenza che confronta diverse strategie di timing di inizio del trattamento con vedolizumab nei pazienti affetti da malattia di Crohn in Italia. Mentre la letteratura esistente si focalizza principalmente sull’efficacia clinica, questo modello integra simultaneamente esiti clinici, utilizzo di risorse e costi sanitari, offrendo una prospettiva più completa delle implicazioni economiche associate alle diverse strategie di avvio della terapia.
Tuttavia, l’analisi presenta alcune limitazioni. La mancanza di dati su alcuni aspetti del trattamento precedente a vedolizumab ha reso necessario il ricorso a un panel di esperti clinici per la validazione di alcuni parametri, tra cui la durata specifica delle terapie nella fase di “Pre-trattamento”. Tuttavia, la scelta metodologica di suddividere i risultati in due scenari distinti (caso base e scenario alternativo) consente di valutare in modo trasparente l’impatto delle assunzioni modellistiche: il caso base, infatti, risulta metodologicamente più robusto, permettendo di limitare l’influenza delle ipotesi considerate nello scenario alternativo. Inoltre, le assunzioni sulla durata delle terapie nei pazienti late CD potrebbero aver portato a una sottostima del burden reale della malattia, non riflettendo pienamente la complessità del percorso terapeutico nei pazienti con lunga storia clinica. Futuri studi sperimentali e osservazionali su popolazioni naïve al trattamento saranno utili per confermare questi risultati.
Inoltre, l’analisi costo-conseguenza presenta alcune fonti di incertezza che potrebbero influenzare l’interpretazione dei risultati. Una prima dimensione riguarda l’incertezza parametrica, in particolare i valori di probabilità di risposta e remissione endoscopica, che derivano da un solo studio clinico [10,11]. Sebbene tali dati rappresentino la miglior evidenza disponibile, variazioni nei tassi di risposta potrebbero modificare l’entità del beneficio associato all’inizio anticipato di vedolizumab. Un’ulteriore fonte di incertezza è rappresentata dai costi sanitari diretti adottati: tali valori possono variare tra regioni e centri italiani e potrebbero non riflettere in maniera uniforme la pratica clinica nazionale.
Vi è inoltre incertezza strutturale legata alle assunzioni del modello, come l’orizzonte temporale, la scelta degli outcome e la modalità di rappresentare le differenze tra strategie di timing (early vs late). Alcune semplificazioni, necessarie per mantenere trasparenza e replicabilità, potrebbero non cogliere completamente la complessità del percorso terapeutico del paziente con CD.
Oltre alle limitazioni già menzionate, è opportuno considerare ulteriori aspetti metodologici che potrebbero influenzare l’interpretazione dei risultati. In primo luogo, l’assenza di studi clinici condotti su popolazioni sovrapponibili ha impedito la realizzazione di un confronto diretto tra diverse molecole per il trattamento della CD. Tuttavia, la crescente adozione di vedolizumab nella pratica clinica e il suo posizionamento nelle linee guida internazionali ne confermano la rilevanza come oggetto di valutazione dedicata [5]. In virtù di queste considerazioni, l’analisi è stata focalizzata esclusivamente su vedolizumab, al fine di garantire coerenza metodologica e pertinenza clinica rispetto alla popolazione target. Il modello si basa su dati di efficacia derivati da un singolo studio clinico (LOVE-CD [10,11]), il cui disegno e popolazione potrebbero non riflettere pienamente la variabilità osservata nella pratica clinica quotidiana. L’assenza di dati real-world limita la generalizzabilità dei risultati, soprattutto in contesti assistenziali eterogenei. In secondo luogo, il modello assume una progressione lineare del percorso terapeutico, suddiviso in fasi discrete, che potrebbe semplificare eccessivamente la complessità clinica della CD, caratterizzata da fluttuazioni, recidive e risposte variabili al trattamento. Inoltre, la stima dei costi indiretti si basa su parametri medi e su assunzioni di produttività che, pur fondate su fonti ufficiali, potrebbero non cogliere appieno le differenze individuali legate al tipo di occupazione, al contesto socioeconomico e alla gravità della malattia. Va inoltre sottolineato che, sebbene lo studio LOVE-CD [10,11] rappresenti una fonte solida e metodologicamente rigorosa, è stato condotto in contesti internazionali europei senza il coinvolgimento specifico di centri italiani. Di conseguenza, potrebbero esistere delle differenze nei criteri di eleggibilità e nelle regole di rimborsabilità dei farmaci biologici rispetto alla normativa vigente in Italia [26]. Tuttavia, per garantire l’attinenza dei risultati al contesto nazionale, questa potenziale discrepanza è stata valutata mediante il coinvolgimento di un panel multidisciplinare di esperti clinici e farmacisti ospedalieri. Il gruppo di esperti ha confermato la pertinenza e l’applicabilità dei dati dello studio LOVE-CD [10,11] alla realtà italiana. In particolare, è stato sottolineato che, in Italia, i risultati del presente studio sono particolarmente rilevanti soprattutto per i pazienti con CD moderata-severa che presentano intolleranza o controindicazioni agli anti-TNF, per i quali vedolizumab rappresenta una valida opzione terapeutica di prima linea di trattamento con biologici con rimborsabilità garantita dal SSN [26]. Tale validazione ha rafforzato la scelta metodologica di utilizzare LOVE-CD [10,11] come base per il modello, garantendo una buona aderenza alla pratica clinica nazionale. Infine, il modello non considera le potenziali differenze di accesso e disponibilità dei farmaci biologici tra regioni italiane, che potrebbero influenzare l’applicabilità dei risultati a livello nazionale. Tali disomogeneità, se non adeguatamente affrontate, rischiano di amplificare le disparità di trattamento e di limitare l’efficacia delle strategie di ottimizzazione proposte.
Nonostante tali limiti, questa analisi offre un contributo originale e rigoroso a supporto delle decisioni di allocazione delle risorse. I risultati ottenuti promuovono una riflessione più ampia sull’ottimizzazione del percorso terapeutico nella CD e sul valore del tempismo terapeutico nella pratica clinica, suggerendo che un intervento precoce con vedolizumab possa tradursi in benefici tangibili sia per il paziente sia per il sistema sanitario. Nel complesso, tutte e tre le classi di biologici approvate per il trattamento della CD risultano più efficaci quando somministrate precocemente nel decorso della malattia [11]. Attualmente, i clinici scelgono il trattamento (di solito in un processo decisionale condiviso con il paziente) in base alla gravità della malattia, alle manifestazioni extraintestinali, alle comorbidità e ai costi [11]. È in corso una ricerca intensiva per validare biomarcatori che possano guidare la scelta terapeutica basata su caratteristiche biologiche piuttosto che cliniche, come nel trial OMICROHN che utilizza profili di metilazione del sangue periferico [11].
Conclusioni
L’analisi presentata evidenzia come l’introduzione precoce di vedolizumab nel trattamento della CD moderata-severa possa rappresentare una strategia clinicamente efficace ed economicamente sostenibile. I risultati ottenuti, sia nel caso base sia nell’analisi di scenario, mostrano una riduzione significativa dei costi totali per paziente, una maggiore probabilità di remissione e un impatto positivo anche in termini di costi indiretti e produttività. Tali evidenze rafforzano il razionale per un ripensamento delle attuali modalità di accesso alle terapie biologiche, promuovendo un approccio più tempestivo e personalizzato. In un contesto sanitario caratterizzato da vincoli economici e disomogeneità organizzative, il presente modello offre uno strumento utile per supportare decisioni allocative basate su evidenze, contribuendo a migliorare l’efficienza del sistema e la qualità dell’assistenza. La valorizzazione del timing terapeutico emerge come un elemento chiave per ottimizzare gli esiti clinici e ridurre il burden economico della malattia, con potenziali benefici per pazienti, clinici e decisori.
Funding
The study was made possible by an unconditional grant from Takeda.
Conflict of interest
C.E., A.M., A.M., R.M., M.V.L. e M.P. received a grant from Takeda to participate in this study.
R.B., I.B. e L.V. are employees of a consultancy firm that received funding from Takeda for this project.
R.V. is an employee of Takeda Italia S.p.A., which financially supported the submitted work, and does not hold stock options.
M.V.L. has received speaking fees from Ferring, Takeda, Abbvie, Janssen; travel grants from Takeda and Abbvie; research support from Takeda and Janssen.
M.P. has received speaking fees, advisory board honoraria, or acted as principal investigator for AbbVie, Celltrion, Ferring, Biogen, Johnson & Johnson, Lilly, MSD, Pfizer, Sandoz, and Takeda.
The other authors declare that they have no other conflicts of interest in relation to this work.
Bibliografia
1.Cockburn E, Kamal S, Chan A, et al. Crohn’s disease: an update. Clin Med (Northfield Il) 2023;23:549–57; https://doi.org/10.7861/CLINMED.2023-0493
2.Clinton JW, Cross RK. Personalized Treatment for Crohn’s Disease: Current Approaches and Future Directions. Clin Exp Gastroenterol. 2023;16:249-276; https://doi.org/10.2147/CEG.S360248
3.CADTH Technology Review: Optimal Use 360 Report Appropriate Pharmacotherapy for Inflammatory Bowel Disease. Available at https://canadacommons.ca/artifacts/34115006/appropriate-pharmacotherapy-for-inflammatory-bowel-disease/35014674/ (last accessed December 2025)
4.NICE. Crohn’s disease: management. NICE guideline 2023. Available at: https://www.nice.org.uk/guidance/ng129 (last accessed december 2025)
5.Gordon H, Minozzi S, Kopylov U, et al. ECCO Guidelines on Therapeutics in Crohn’s Disease: Medical Treatment. J Crohn’s Colitis. 2024;18:1531–55; https://doi.org/10.1093/ECCO-JCC/JJAE091
6.Singh S, Proctor D, Scott FI, et al. AGA Technical Review on the Medical Management of Moderate to Severe Luminal and Perianal Fistulizing Crohn’s Disease. Gastroenterology. 2021;160:2512-2556.e9; https://doi.org/10.1053/j.gastro.2021.04.023
7.Macaluso FS, Papi C, Orlando A, et al. Use of biologics for the management of Crohn’s disease: IG-IBD clinical guidelines based on the GRADE methodology. Dig Liver Dis. 2023;55:442–53; https://doi.org/10.1016/j.dld.2023.01.155
8.Noor NM, Lee JC, Bond S, et al. A biomarker-stratified comparison of top-down versus accelerated step-up treatment strategies for patients with newly diagnosed Crohn’s disease (PROFILE): a multicentre, open-label randomised controlled trial. Lancet Gastroenterol Hepatol. 2024;9:415–27; https://doi.org/10.1016/S2468-1253(24)00034-7
9.Khanna R, Bressler B, Levesque BG, et al. Early combined immunosuppression for the management of Crohn’s disease (REACT): A cluster randomised controlled trial. Lancet. 2015;386:1825–34; https://doi.org/10.1016/S0140-6736(15)00068-9
10.Oldenburg L, Baert F, Bossuyt P, et al. DOP085 Higher clinical remission and endoscopic response with vedolizumab in early versus late Crohn’s disease: data from the LOVE-CD trial. J Crohns Colitis. 2025;19(Supplement_1):i240–i241; https://doi.org/10.1093/ecco-jcc/jjae190.0124
11.D’Haens GR, Löwenberg M, Baert F, et al. Vedolizumab in early and late Crohn’s disease (LOVE-CD): a phase 4 open-label cohort study. Lancet Gastroenterol Hepatol. 2026;11(1):12-21. https://doi.org/10.1016/S2468-1253(25)00233-X
12.Armeni P, Compagnucci E, Fiorino G, et al. Una valutazione economica di due sequenze terapeutiche nel trattamento di prima linea della rettocolite ulcerosa attiva da moderata a grave in Italia. AboutOpen.2024;11: 21-29; https://doi.org/10.33393/ao.2024.2893
13.Salcedo J, Hill-McManus D, Hardern C, et al. Cost-Effectiveness of Vedolizumab as a First-Line Advanced Therapy Versus Adalimumab Treatment Sequences for Ulcerative Colitis in Italy. PharmacoEconomics Open. 2024;8:701–14; https://doi.org/10.1007/S41669-024-00497-4.
14.Agenzia Italiana del Farmaco (AIFA). DETERMINA 6 luglio 2016. Rettifica della determina n. 459/2016 del 31 marzo 2016, relativa alla riclassificazione del medicinale per uso umano «Entyvio», ai sensi dell’articolo 8, comma 10, della legge 24 dicembre 1993, n. 537. (Determina n. 897/2016). (16A05288) (GU Serie Generale n.170 del 22-07-2016). Available at: https://www.gazzettaufficiale.it/atto/serie_generale/caricaDettaglioAtto/originario?atto.dataPubblicazioneGazzetta=2016-07-22&atto.codiceRedazionale=16A05288 (last accessed October 2025)
15.Page MJ, McKenzie JE, Bossuyt PM, et al. The PRISMA 2020 statement: an updated guideline for reporting systematic reviews. BMJ. 2021;372; https://doi.org/10.1136/BMJ.N71
16.Agenzia Italiana del Farmaco (AIFA). Elenco dei farmaci di classe A e H. Available at: https://www.aifa.gov.it/liste-farmaci-a-h (last accessed december 2025)
17.Colombo GL, Di Matteo S, Martinotti C, et al. Il costo ombra dei farmaci corticosteroidi nei pazienti con colite ulcerosa in Italia: un’analisi di impatto sul budget. ClinicoEconomics. 2023;18:49–60
18.Ministero della Salute. Tariffe delle prestazioni ospedaliere. Supplemento n.8, Gazzetta Ufficiale n.23,2013. 2013;Allegato 1
19.Database - Eurostat. Available at: https://ec.europa.eu/eurostat/data/database (last accessed September 2025)
20.Holko P, Kawalec P, Sajak-Szczerba M, et al. Indirect Costs of Inflammatory Bowel Diseases: A Comparison of Patient-Reported Outcomes Across 12 European Countries. Inflamm Bowel Dis. 2022;29:752; https://doi.org/10.1093/IBD/IZAC144
21.Degli Esposti L, Daperno M, Dovizio M, et al. A retrospective analysis of treatment patterns, drug discontinuation and healthcare costs in Crohn’s disease patients treated with biologics. Dig Liver Dis. 2023;55:1214–20; https://doi.org/10.1016/j.dld.2023.04.010
22.Jongsma MME, Aardoom MA, Cozijnsen MA, et al. First-line treatment with infliximab versus conventional treatment in children with newly diagnosed moderate-to-severe Crohn’s disease: an open-label multicentre randomised controlled trial. Gut. 2022;71:34–42; https://doi.org/10.1136/GUTJNL-2020-322339
23.Marchetti M, Liberato NL, Di Sabatino A, et al. Cost-effectiveness analysis of top-down versus step-up strategies in patients with newly diagnosed active luminal Crohn’s disease. Eur J Health Econ. 2013;14:853–61; https://doi.org/10.1007/S10198-012-0430-7
24.Afzali A, Rubin DT, Danese S, et al. DOP060 Early disease efficacy of guselkumab therapy in biologic-naïve patients with moderately to severely active Crohn’s disease: Post-hoc analysis from the phase 3 GALAXI 2 & 3 studies. J Crohn’s Colitis. 2025;19:i202–3; https://doi.org/10.1093/ECCO-JCC/JJAE190.0099
25.Sands BE, Irving PM, Hoops T, et al. Ustekinumab versus adalimumab for induction and maintenance therapy in biologic-naive patients with moderately to severely active Crohn’s disease: a multicentre, randomised, double-blind, parallel-group, phase 3b trial. Lancet. 2022;399:2200–11; https://doi.org/10.1016/S0140-6736(22)00688-2
26.Aggiornamento della scheda di prescrizione cartacea dei farmaci per la malattia di Crohn per linee di trattamento successive agli inibitori del TNF-ALFA. (Determina n. 6/2024). (24A02549) (GU Serie Generale n.118 del 22-05-2024) n.d.