Farmeconomia. Health economics and therapeutic pathways 2026; 27(1): 1-12
https://doi.org/10.7175/fe.v27i1.1606
Original research
Analisi epidemiologica e burden economico delle neoplasie gastriche e della giunzione gastroesofagea in Italia
Paolo Sciattella 1, Angela Ragonese 1, Rossana Berardi 2, Maria Di Bartolomeo 3, Evaristo Maiello 4, Paolo Di Rienzo 5, Fausto Bartolini 6, Andrea Marcellusi 7
1 Economic Evaluation and HTA (EEHTA), CEIS, Faculty of Economics, University of Rome “Tor Vergata”, Rome, Italy
2 Clinica Oncologica, Università Politecnica delle Marche – AOU delle Marche, Ancona, Italy
3 Già presso Oncologia Medica, Fondazione IRCCS Istituto Nazionale dei Tumori, Milan, Italy
4 Oncology Unit, Foundation IRCCS Casa Sollievo della Sofferenza, San Giovanni Rotondo (FG), Italy
5 Astellas Pharma Italia S.p.A, Milan, Italy
6 USL Umbria 2, Terni, Italy
7 Department of Pharmaceutical Science (DISFARM), University of Milan, Milan, Italy
Abstract
OBJECTIVES: To estimate the epidemiological distribution and economic impact of gastric and gastroesophageal junction neoplasms in Italy.
METHODS: Retrospective transversal and longitudinal analyses were conducted using the Italian Hospital Discharge Records from 2010 to 2019, and the administrative databases of the Umbria 2 Local Health Unit for the period 2014–2018. Patients were stratified by disease stage. Incidence, prevalence, in-hospital mortality, and progression patterns were estimated. Cost analyses included hospitalizations, outpatient specialist services, and pharmaceutical expenditures, based on regional tariffs. The methodology and findings were validated through two structured discussions with Key Opinion Leaders from northern, central, and southern Italy.
RESULTS: The national incidence and mortality decreased over time, while prevalence showed a peak in 2017. A marked regional variability in hospitalization rates was noted, reflecting differences in healthcare practices rather than underlying epidemiology. The trend toward decreased mortality was not confirmed by the analysis in Umbria 2 Health Authority, which accounted also for non-hospital mortality. Average annual per-patient costs borne by the Italian National Health Service (NHS) were €12,797, €18,505, and €15,173 for localized, locally advanced, and metastatic disease, respectively. Hospitalization costs accounted for over 88% of expenses. One-year mortality reached 74% in the metastatic group. As the period considered predates the widespread adoption of high-cost targeted therapies and immunotherapies, current costs are likely underestimated.
CONCLUSIONS: Gastric and gastroesophageal junction cancers remain a significant burden for the Italian NHS in terms of both clinical outcomes and healthcare spending. This study offers an integrated national and regional perspective on the real-world impact of these diseases, reinforcing the need for improved data integration, early detection strategies, and resource planning tailored to future therapeutic developments.
Keywords
Gastric cancer; Gastroesophageal junction cancer; Epidemiology; Healthcare costs; Administrative data; Real-world evidence
Received: 13 October 2025
Accepted: 6 February 2026
Published: 2 March 2026
Introduzione
Il carcinoma gastrico è una neoplasia a comportamento aggressivo, caratterizzata da una prognosi sfavorevole a causa dell’elevata incidenza di recidive nonostante interventi chirurgici radicali e dalla tendenza a essere rilevata in stadi già avanzati della malattia [1].
I dati dell’Organizzazione Mondiale della Sanità (World Health Organization – WHO) relativi al 2022 riportano che si colloca al quinto posto a livello globale sia per incidenza sia per mortalità [2]. L’incidenza è decisamente più alta nel continente asiatico [2].
Secondo i dati più recenti de “I numeri del cancro”, una pubblicazione annuale basata sul registro AIRTUM [3], in Italia sono state stimate circa 14.105 nuove diagnosi, prevalentemente nel sesso maschile. È stato calcolato che circa 72.900 persone vivono in Italia dopo una diagnosi di carcinoma gastrico [3].
Si tratta di uno dei tumori a prognosi più sfavorevole, con una sopravvivenza a 5 anni in Italia pari al 32% [3].
I tumori dello stomaco si suddividono principalmente in due sedi topografiche: la regione non-cardiale, localizzata nelle porzioni distali dello stomaco, responsabile di circa l’82% dei casi, e la regione cardiale, situata in prossimità della giunzione esofago-gastrica, che interessa circa il 18% dei tumori gastrici [4].
Negli ultimi decenni sono state osservate diminuzioni costanti dell’incidenza e dei tassi di mortalità e si prevede che la tendenza continuerà in futuro [5,6]. Questo fenomeno si spiega considerando i fattori di rischio. Sebbene entrambe le sedi condividano alcuni fattori di rischio – come il fumo, l’alcol in quantità elevate e il consumo di alimenti conservati sotto sale – presentano anche cause eziologiche differenti. Il tumore del cardias è spesso associato al reflusso gastroesofageo e all’obesità, mentre l’infezione da Helicobacter pylori è responsabile di circa il 90% dei tumori non-cardiali [4]. Le infezioni da Helicobacter pylori hanno fatto registrare una diminuzione a causa sia della minor prevalenza del batterio, sia dei miglioramenti nella conservazione del cibo e nell’igiene [4,7]. Il consumo di cibi salati è fortemente diminuito negli ultimi anni principalmente per questioni legate a diete antipertensive.
Tuttavia è emersa negli ultimi anni una tendenza all’aumento dell’incidenza di cancro allo stomaco nella popolazione <50 anni, dipendente anche dalla variazione di abitudini alimentari e dall’obesità [4].
Nonostante questa neoplasia resti tra quelle a prognosi più sfavorevole, l’ultimo decennio ha visto significativi progressi nelle strategie terapeutiche. In particolare, è stata validata l’utilità della terapia perioperatoria nella malattia operabile, così come l’introduzione di un approccio “continuum of care”, basato sull’impiego sequenziale dei diversi trattamenti attivi, nella malattia metastatica ha contribuito a un miglioramento complessivo della prognosi [1]. La personalizzazione della terapia legata al profilo molecolare del tumore, inoltre, comporta una complessità nella gestione del paziente che è in continua evoluzione.
Pertanto, dal punto di vista del consumo delle risorse sanitarie va evidenziato come il costo del trattamento del cancro gastrico sia destinato ad aumentare in modo significativo [8] rendendo di estrema importanza una valutazione dei percorsi di gestione dei pazienti in ognuna delle fasi della patologia.
Nel tentativo di stimare la distribuzione epidemiologica dei pazienti con carcinoma gastrico in Italia si incontra la difficoltà legata alla mancanza di fonti del Servizio Sanitario Nazionale (SSN) che possano mettere in collegamento l’attività ospedaliera e quella ambulatoriale per le terapie mediche e tra le diverse regioni italiane. La presenza di tale collegamento sarebbe particolarmente importante, dal momento che le strategie terapeutiche sviluppate negli ultimi anni stanno spingendo verso la gestione ambulatoriale del paziente oncologico.
Il presente progetto si pone l’obiettivo di stimare la distribuzione epidemiologica dei pazienti (incidenti e prevalenti) gestiti in Italia per il trattamento del carcinoma gastrico non resecabile localmente avanzato e metastatico e i relativi costi a carico del SSN, al fine di fornire informazioni che possano consentire l’allocazione ottimale delle risorse per la gestione di questa patologia.
Metodi
Fonte dei dati
L’analisi è stata condotta utilizzando il flusso nazionale della Scheda di Dimissione Ospedaliera (SDO) relativo al periodo 2009-2019 e i database amministrativi sanitari della Unità Sanitaria Locale (USL) Umbria 2 relativi al periodo 2014-2018, i più recenti disponibili al momento dell’analisi.
Il flusso SDO registra le informazioni relative a tutte le dimissioni da ospedali pubblici e privati presenti sul territorio nazionale.
Per la USL Umbria 2 sono stati considerati i database relativi all’anagrafe assistiti, all’assistenza ospedaliera, alle dispensazioni farmaceutiche erogate in distribuzione diretta, per conto (DPC) e convenzionata e all’assistenza specialistica ambulatoriale e di laboratorio. Le informazioni provenienti dalle diverse fonti sono state integrate mediante procedure di record linkage a livello individuale basate su codice identificativo univoco e anonimo.
L’analisi economica è stata condotta dalla prospettiva del SSN, includendo i costi sanitari diretti sostenuti dal SSN, relativamente ad assistenza ospedaliera, farmaceutica e specialistica ambulatoriale e di laboratorio. Sono stati invece esclusi i costi dei farmaci somministrati in regime ospedaliero o ambulatoriale non registrati nei sistemi informativi regionali disponibili.
Analisi trasversale
Sono stati inclusi nello studio tutti i soggetti con carcinoma gastrico dimessi da specialità per acuti e post-acuti (riabilitazione e lungodegenza), in regime ordinario o day hospital, identificati secondo la classificazione riportata in Tabella I.
|
Stadio di carcinoma gastrico |
Codici inclusi |
Codici esclusi |
|
Localizzato |
ICD9CM 151.xx: diagnosi principale o secondaria di “tumori maligni dello stomaco” |
ICD9CM 196.x-198.x: diagnosi di “tumori maligni secondari” |
|
Localmente avanzato |
Contemporanea presenza dei codici:
|
ICD9CM 197.x-198.x: diagnosi di “tumori maligni secondari degli apparati respiratorio e digerente e di altre sedi non specificate” |
|
Metastatico |
Contemporanea presenza dei codici:
|
Tabella I. Pazienti inclusi ed esclusi nell’analisi sulla base dei codici di diagnosi
Per ogni anno è stato calcolato il numero di pazienti dimessi, il numero di pazienti deceduti in ospedale e il numero di pazienti persi al follow-up. Non avendo informazioni relative alla mortalità extra-ospedaliera, sono stati considerati come “persi al follow-up” i pazienti per i quali non sono stati registrati ricoveri negli anni successivi al ricovero di selezione né è stato registrato un decesso.
Per ogni anno in studio, i pazienti selezionati sono stati definiti incidenti se negli anni precedenti non erano state registrate ospedalizzazioni per tumore gastrico. I risultati emersi dall’analisi dei pazienti incidenti sono stati confrontati con i dati provenienti da registro AIRTUM [9–17] ed è stato calcolato lo scostamento in termini assoluti e relativi.
Il numero di pazienti prevalenti, a fine anno (t), è stato calcolato secondo la formula [18]:
Prevalenti t = Prevalenti t-1 + Incidenti t – Decessi t – Persi al follow-up t
Per avere una stima della variabilità regionale dei pazienti selezionati, è stato calcolato il tasso di ospedalizzazione per carcinoma gastrico, rapportando, per ogni regione, il numero di soggetti ospedalizzati nel 2019 alla popolazione residente secondo i dati ISTAT [19].
La metodologia di analisi è stata replicata sui pazienti assistiti nella USL Umbria 2, considerando anche la mortalità generale proveniente da anagrafe.
Analisi longitudinale
Analisi nazionale
Sono stati selezionati tutti i pazienti con un primo ricovero per carcinoma gastrico nel periodo 2010-2014; qualora un paziente avesse avuto più ricoveri nel periodo di arruolamento, il primo ricovero è stato selezionato come quello di arruolamento e definito “ricovero indice”. I pazienti identificati, sono stati seguiti per un follow-up minimo di 5 anni, durante il quale sono stati stimati sia la presenza di progressione della malattia sia i tempi alla progressione da carcinoma localizzato a carcinoma localmente avanzato, da carcinoma localizzato a carcinoma metastatico e da carcinoma localmente avanzato a carcinoma metastatico.
Analisi relative alla ASL Umbria 2
L’analisi è stata replicata individuando la coorte dei pazienti con un primo ricovero per carcinoma gastrico nel periodo 2014-2017. Ogni paziente è stato seguito per un periodo di un anno, con fine del follow-up fissata al 31 dicembre 2018, durante il quale è stata stimata la spesa a carico del SSN sommando i costi dei ricoveri, del consumo di farmaci e delle visite specialistiche. La valorizzazione delle prestazioni è stata effettuata considerando i tariffari per l’assistenza ospedaliera e specialistica ambulatoriale e il prezzo al pubblico per i farmaci [11,12].
Le analisi sono state stratificate in base alla classificazione dei tumori: carcinoma localizzato, carcinoma localmente avanzato e carcinoma metastatico.
Validazione della metodologia
La metodologia e i risultati delle analisi sono stati validati e discussi durante un focus group a cui hanno partecipato tre Key Opinion Leader (KOL) coinvolti a più livelli nella gestione del tumore gastrico in rappresentanza di strutture del Nord, Centro e Sud Italia. Durante l’incontro i dati di real-world sono stati integrati con l’esperienza di real-life dei partecipanti, consentendo un’interpretazione critica dei principali risultati; particolare attenzione è stata dedicata al setting dei pazienti con malattia metastatica e con tumore localmente avanzato non resecabile. Le considerazioni emerse dal confronto fanno riferimento all’esperienza maturata dai KOL nei rispettivi centri nel periodo compreso tra luglio 2021 e giugno 2022.
Risultati
Analisi trasversale
Analisi nazionale
Il numero di pazienti con un primo ricovero per carcinoma gastrico nel quinquennio 2015-2019 è risultato, in media, pari a circa 13.000 l’anno. Analizzando il trend si nota una sovrastima attesa nei primi anni di analisi, dovuta all’impossibilità di verificare la presenza di pregressi ricoveri, mentre le stime cominciano a essere stabili e maggiormente attendibili a partire dal 2015-2016, con valori pressocché sovrapponibili a quelli del registro AIRTUM, a eccezione dell’anno 2019, per il quale “I numeri del cancro” [17] indicano una crescita repentina (1.600 pazienti, +12%) rispetto all’anno precedente, mentre il dato SDO conferma il trend di leggera discesa degli anni precedenti (Figura 1).
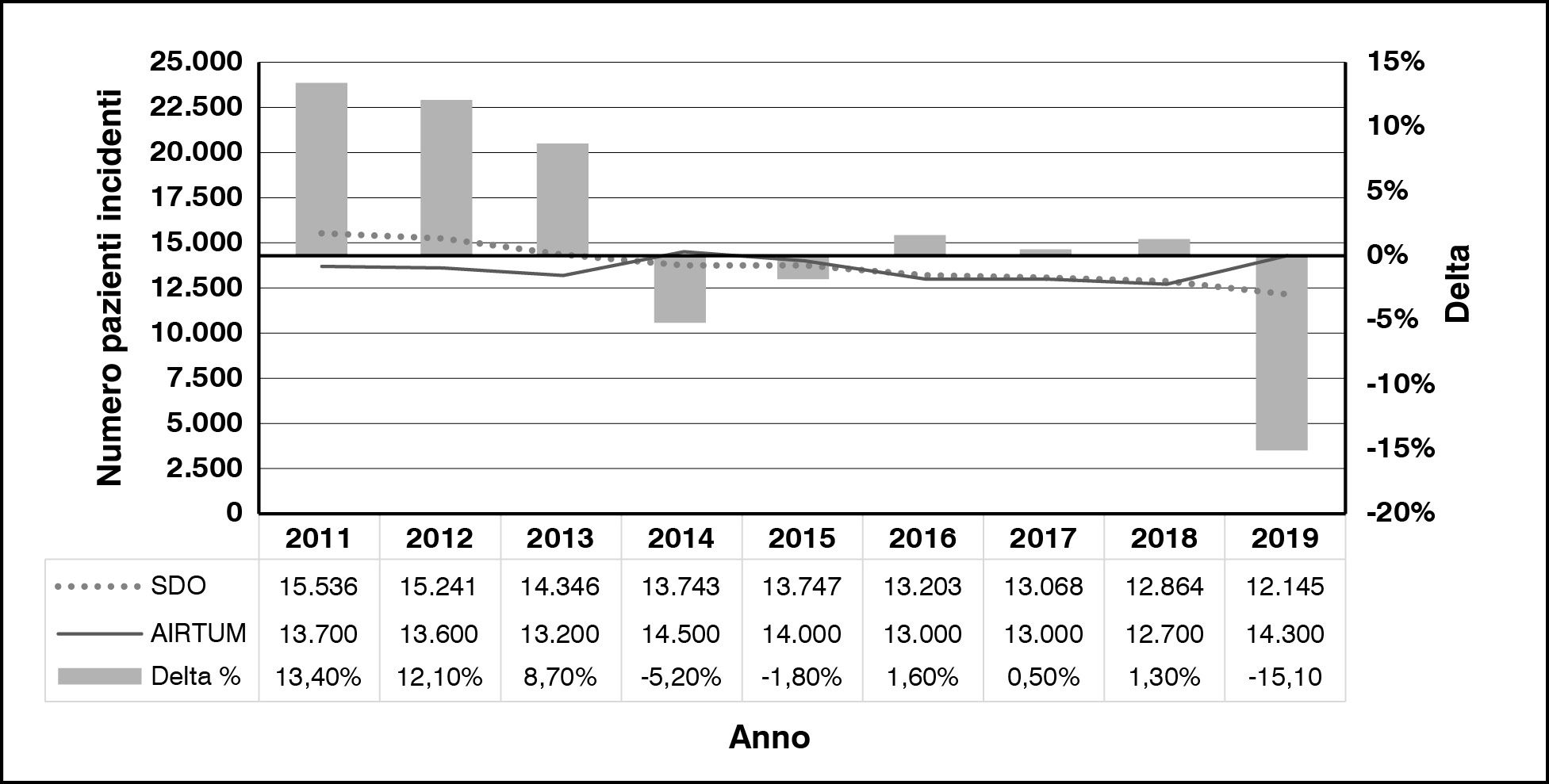
Figura 1. Confronto dei dati relativi ai pazienti con carcinoma gastrico incidenti in Italia tra le due diverse fonti considerate: le Schede di Dimissione Ospedaliera (SDO) e “I numeri del cancro” (AIRTUM) [9–17]
L’analisi delle SDO ha permesso di calcolare, oltre ai pazienti incidenti, anche i pazienti prevalenti, il numero di decessi e di pazienti persi al follow-up. Le Tabelle II e III mostrano tali dati rispettivamente per i pazienti totali e per i pazienti con carcinoma gastrico localmente avanzato o metastatico, mentre i dettagli relativamente alle sottopopolazioni separate di pazienti con carcinoma gastrico localizzato, localmente avanzato e metastatico sono riportati nel Materiale Supplementare rispettivamente nelle Tabelle S1, S2 e S3.
|
Anno |
Pazienti incidenti |
Pazienti ospedalizzati |
Decessi |
Persi al follow-up |
Pazienti prevalenti (fine anno) |
Ricoveri |
|
2015 |
13.747 |
17.394 |
2.917 |
7.238 |
37.505 |
26.958 |
|
2016 |
13.203 |
16.844 |
2.812 |
7.304 |
40.592 |
25.886 |
|
2017 |
13.068 |
16.559 |
2.735 |
7.738 |
43.187 |
25.148 |
|
2018 |
12.864 |
16.333 |
2.717 |
8.580 |
44.754 |
24.209 |
|
2019 |
12.145 |
15.548 |
2.494 |
13.054 |
41.351 |
23.540 |
Tabella II. Pazienti con carcinoma gastrico in Italia tra il 2015 e il 2019
|
Anno |
Pazienti incidenti |
Decessi |
Persi al follow-up |
Pazienti prevalenti (fine anno) |
|
2015 |
5.802 |
1.603 |
3.705 |
7.277 |
|
2016 |
5.428 |
1.591 |
3.598 |
7.516 |
|
2017 |
5.301 |
1.478 |
3.654 |
7.685 |
|
2018 |
4.861 |
1.432 |
3.637 |
7.477 |
|
2019 |
4.642 |
1.279 |
5.578 |
5.262 |
Tabella III. Pazienti con carcinoma gastrico localmente avanzato o metastatico in Italia tra il 2015 e il 2019
L’analisi ha evidenziato una significativa variabilità regionale, con valori tendenzialmente più alti nelle regioni centrali (Figura 2).
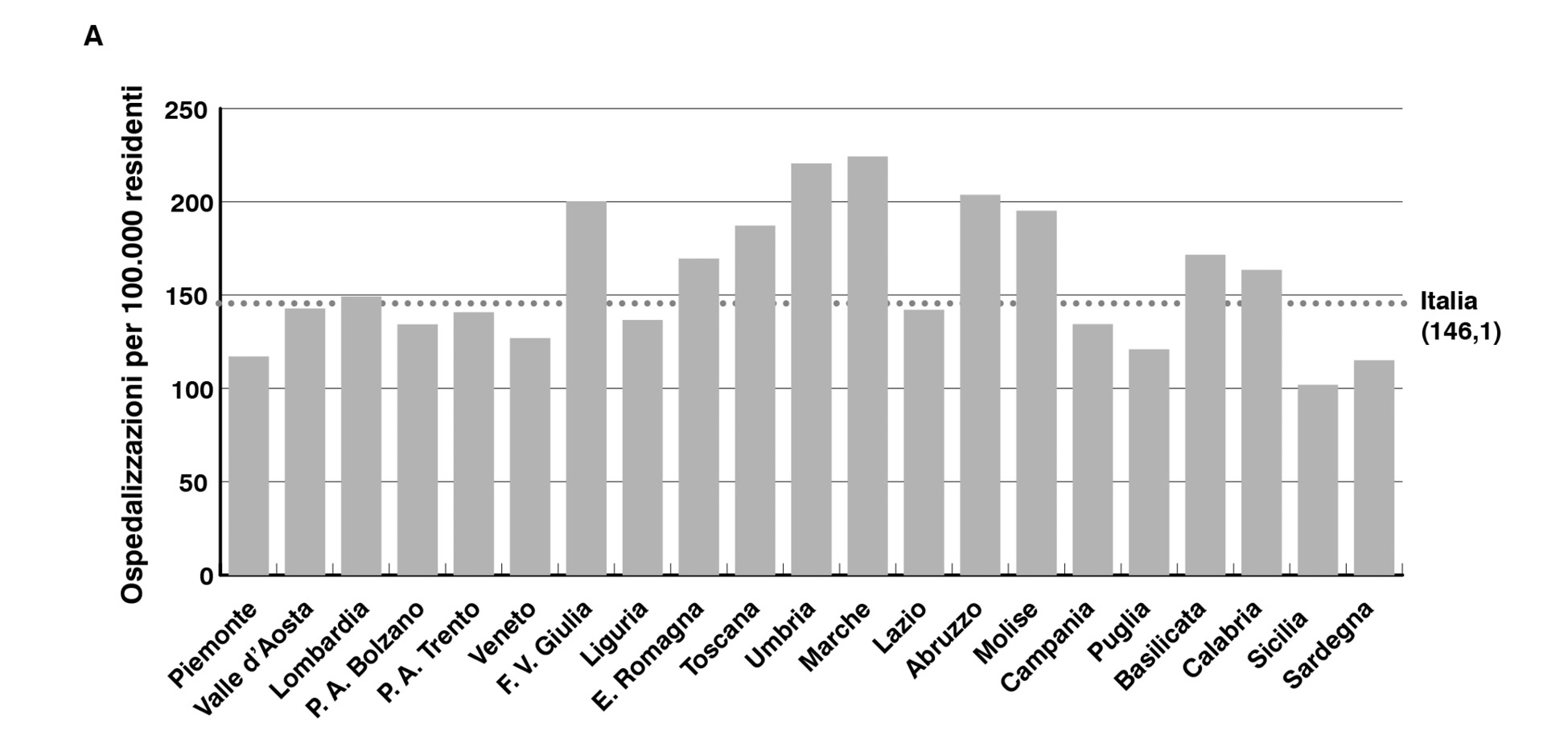
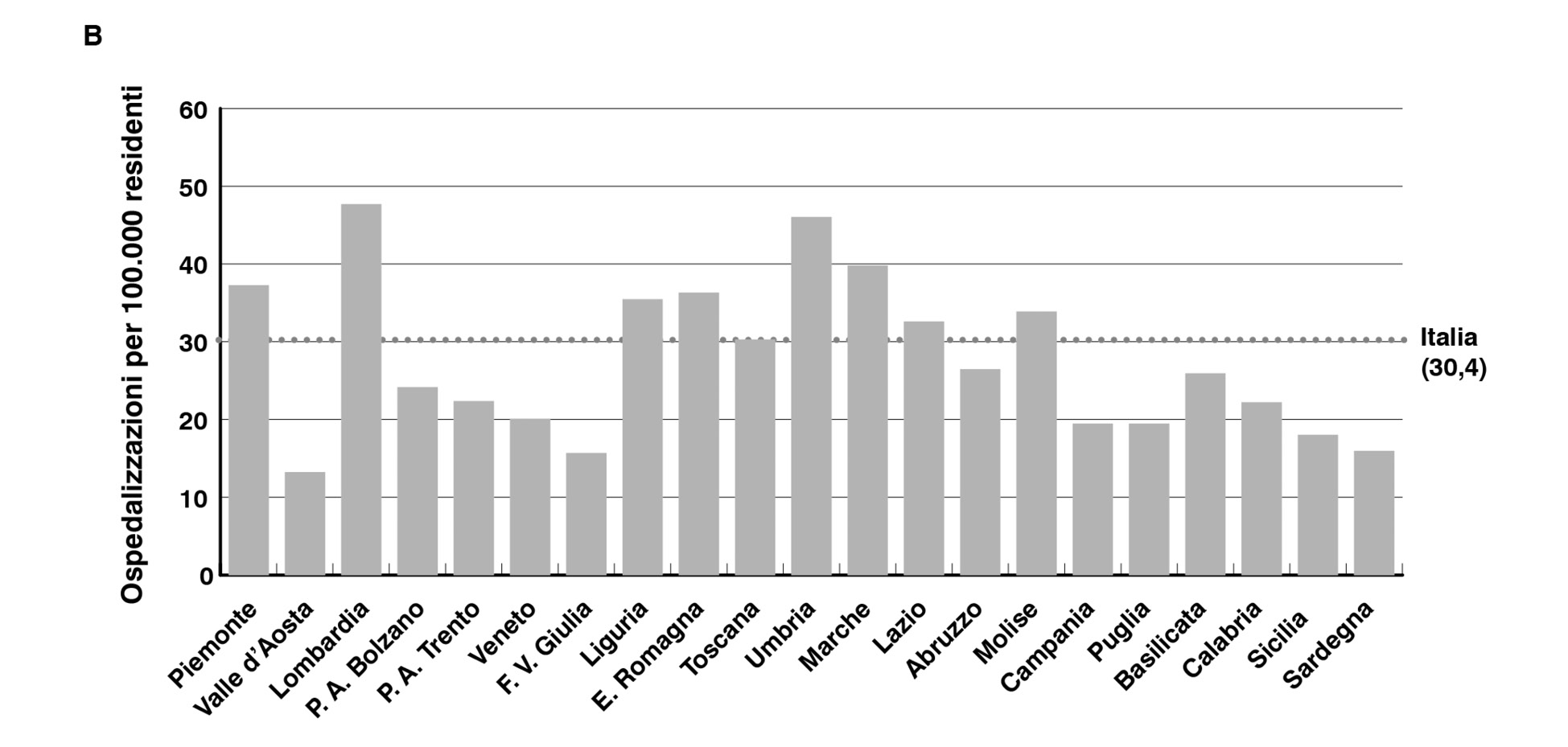
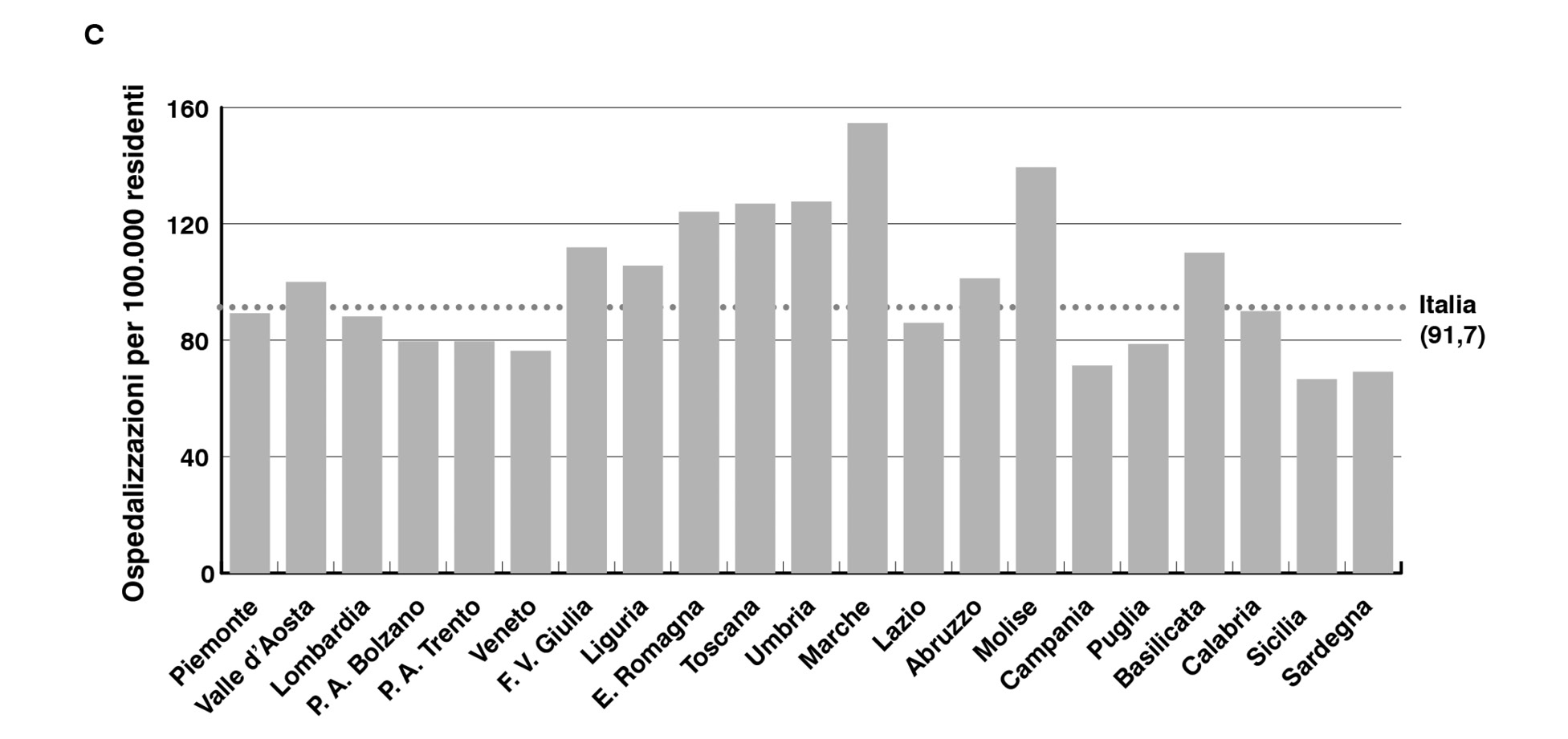
Figura 2. Tasso di ospedalizzazione per regione di residenza. Valori per 100.000 residenti (Italia 2019). A: carcinoma gastrico localizzato; B: carcinoma gastrico localmente avanzato; C: carcinoma gastrico metastatico
Analisi relative alla ASL Umbria 2
L’analisi condotta sugli assistiti della ASL Umbria 2 (Figura S1) conferma i risultati dell’analisi effettuata sulle SDO nazionali in termini di prevalenza, mentre la mortalità, accertata mediante l’anagrafe assistiti, che, al contrario delle SDO, traccia tutti i decessi e non solo quelli avvenuti in ospedale, non ricalca il trend in forte diminuzione rilevato a livello nazionale (Figura S1B).
Si riduce, inoltre, la quota di pazienti persi al follow-up, presenti quasi esclusivamente nell’ultimo anno di analisi, grazie alle maggiori informazioni disponibili per individuare i decessi.
Analisi longitudinale
Analisi nazionale
Sono stati selezionati 50.748 pazienti con un primo ricovero per carcinoma gastrico nel periodo 2010-2014 (Tabella IV).
|
Anno di arruolamento |
Soggetti |
No progressione |
Progressione localizzato → LA |
Progressione localizzato → metast. |
Progressione LA → metast. |
|
2010 |
12.050 |
80,8% |
4,0% |
10,6% |
4,5% |
|
2011 |
10.343 |
81,9% |
4,5% |
9,5% |
4,2% |
|
2012 |
10.019 |
82,3% |
4,2% |
9,3% |
4,3% |
|
2013 |
9.395 |
83,4% |
3,9% |
8,2% |
4,4% |
|
2014 |
8.941 |
83,1% |
4,2% |
8,8% |
3,9% |
|
Totale |
50.748 |
82,2% |
4,2% |
9,4% |
4,3% |
Tabella IV. Pazienti ospedalizzati con primo ricovero per carcinoma gastrico localizzato, seguiti per un follow-up minimo di 5 anni in Italia tra il 2010 e il 2014
LA = localmente avanzato; metast. = metastatico
Nel corso del follow-up, per il 17,9% dei pazienti è stata osservata una progressione di malattia: il 4,2% da carcinoma localizzato a carcinoma localmente avanzato, il 9,4% da carcinoma localizzato a carcinoma metastatico e il restante 4,3% progredisce in carcinoma localmente avanzato e successivamente in carcinoma metastatico.
Il tempo mediano alla progressione è riportato nella Tabella V.
|
Tempo alla progressione (giorni) |
Progressione localizzato → LA (n=4.290) |
Progressione |
Progressione LA → metast. (n=660) |
|
Media |
214 |
359 |
427 |
|
Mediana |
71 |
174 |
283 |
|
IQR |
32-209 |
46-480 |
126-584 |
Tabella V. Tempo alla progressione calcolato sui soli pazienti con progressione
IQR = range interquartile; LA: localmente avanzato; metast. = metastatico
Analisi relative alla ASL Umbria 2
Nel periodo 2014-2017 sono stati selezionati 431 assistiti con un primo ricovero per carcinoma gastrico, di cui 182 con carcinoma gastrico localizzato, 66 con carcinoma gastrico localmente avanzato e 183 con carcinoma gastrico metastatico.
La mortalità a un anno è risultata pari al 38% (69 decessi su 182) per i carcinomi localizzati, al 26% (17 decessi su 66) per i carcinomi localmente avanzati e al 74% (136 decessi su 183) per i carcinomi metastatici.
La spesa media a carico del SSN è risultata pari a €12.797 per paziente con carcinoma primario, a €18.504 per paziente con carcinoma localmente avanzato e €15.174 per paziente con carcinoma metastatico (Figura 3).
1-12-web-resources/image/img01_03a.jpg)
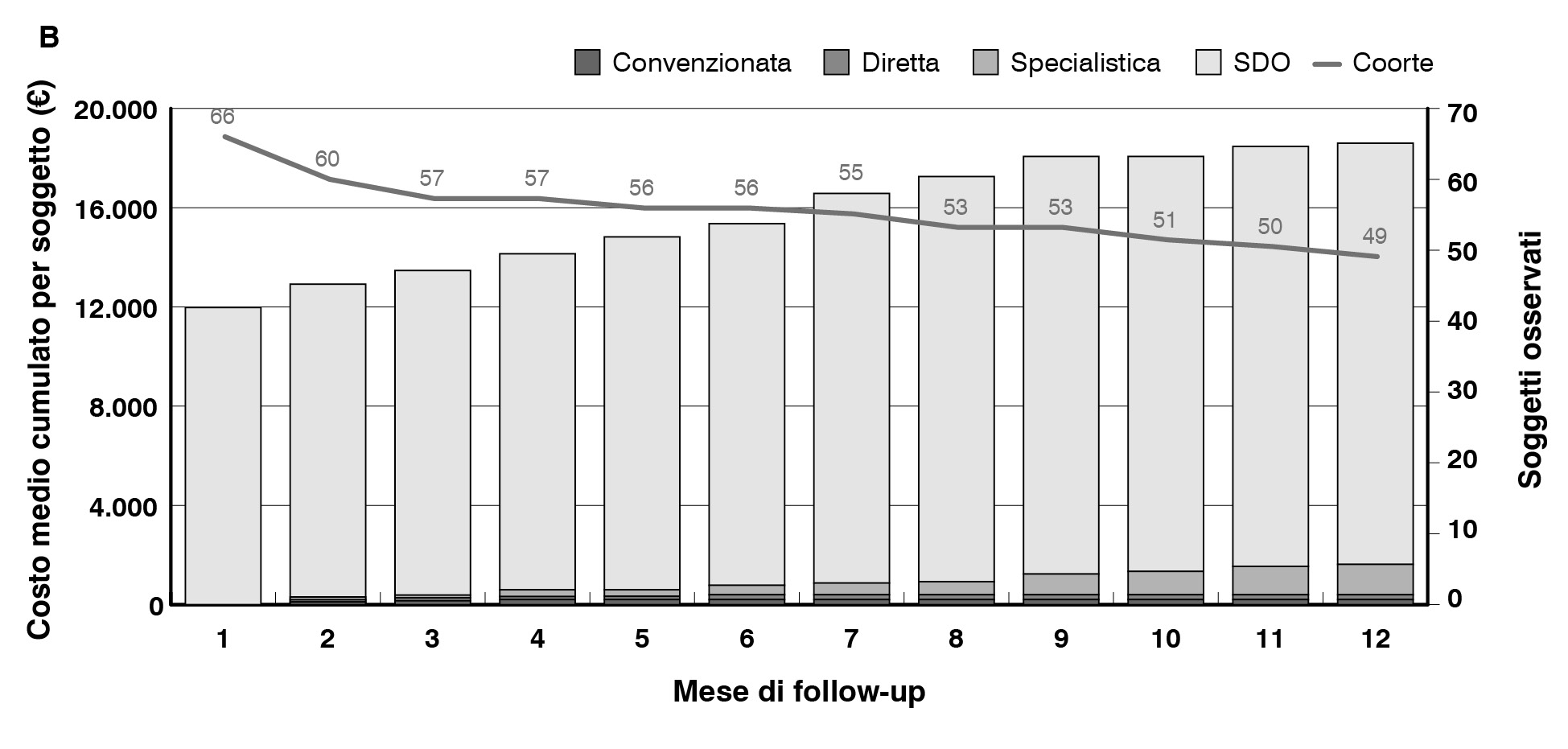
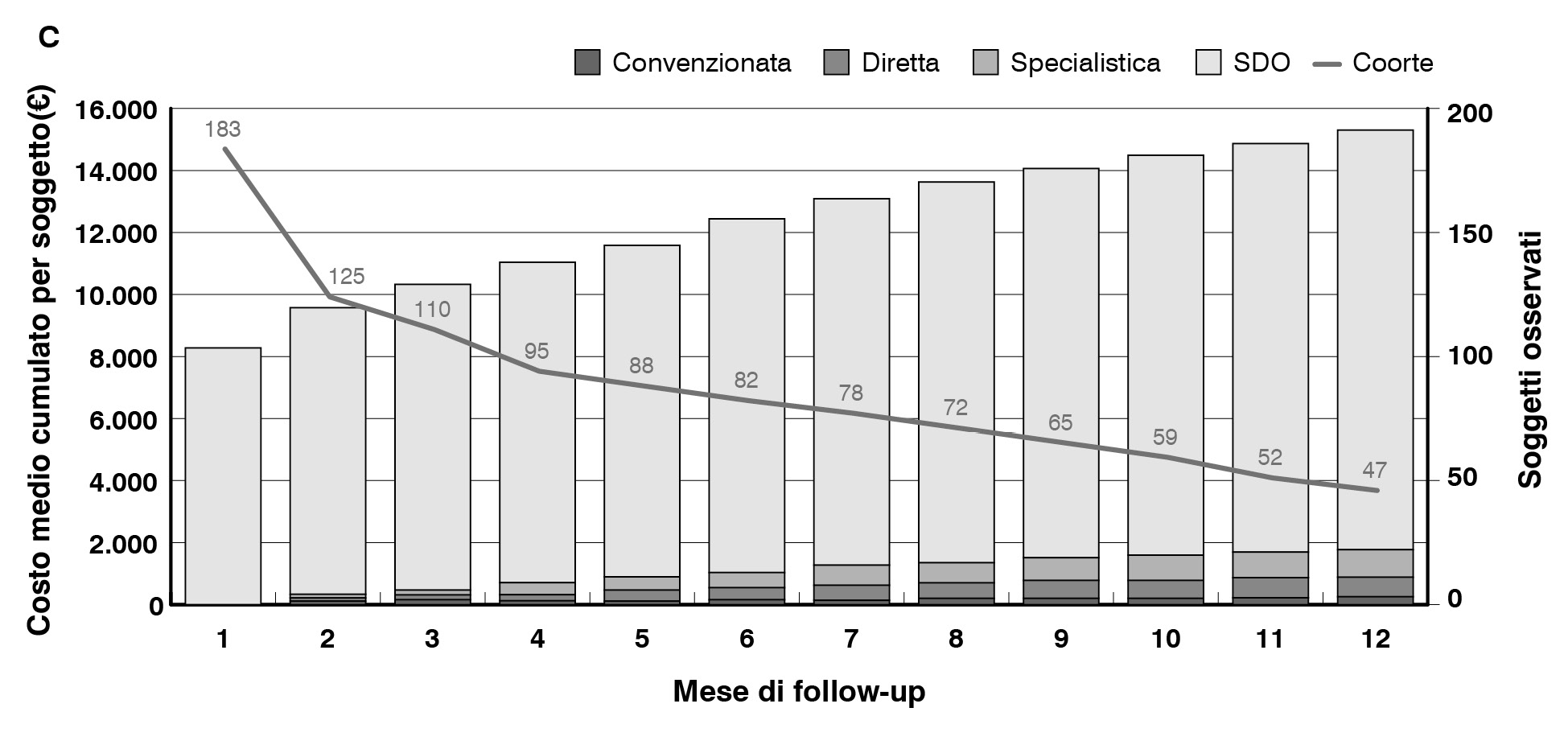
Figura 3. Spesa media annua per paziente nella ASL Umbria 2 nel periodo 2014-2018. A: pazienti con carcinoma gastrico localizzato; B: pazienti con carcinoma gastrico localmente avanzato; C: pazienti con carcinoma gastrico metastatico
Nel dettaglio, la quasi totalità della spesa è relativa all’assistenza ospedaliera che assomma all’88% della spesa per i pazienti con carcinoma primario (50% ricovero indice e 38% riospedalizzazioni) e carcinoma metastatico (46% ricovero indice e 42% riospedalizzazioni) e al 91% (60% ricovero indice e 31% riospedalizzazioni) per i pazienti con carcinoma localmente avanzato. La spesa restante è equidistribuita tra assistenza farmaceutica, relativa a farmaci dispensati per il consumo a domicilio del paziente, e specialistica ambulatoriale.
Nel corso del follow-up di un anno, sono state analizzate la mortalità generale (intra- ed extra-ospedaliera) e il consumo di risorse dei pazienti selezionati, come mostrato in Tabella VI.
|
Carcinoma |
Soggetti (n) |
Spesa (€) |
Spesa farmaceutica (%) |
Spesa specialistica (%) |
Spesa ospedaliera (%) |
||
|
Convenzionata |
Diretta |
Ricovero indice |
Riospedalizzazioni |
||||
|
Localizzato |
182 |
12.797 |
3,2 |
3,0 |
6,3 |
49,8 |
37,7 |
|
Localmente avanzato |
66 |
18.505 |
1,6 |
1,3 |
6,0 |
59,8 |
31,2 |
|
Metastatico |
183 |
15.173 |
2,2 |
4,3 |
5,7 |
45,9 |
41,9 |
Tabella VI. Spesa annua media per paziente con carcinoma gastrico nella ASL Umbria 2 nel periodo 2014-2018
Analisi delle schede riportate dai clinici
La valutazione dell’espressione di HER2 viene effettuata nei pazienti con carcinoma metastatico, trattandosi di un’informazione predittiva per la successiva terapia; nel periodo considerato, circa il 70% dei pazienti ha presentato un carcinoma metastatico HER2-.
Per quanto riguarda il trattamento, la maggior parte dei pazienti (>80%) è risultata eleggibile per una doppietta comprendente un derivato del platino (oxaliplatino). In questo setting di pazienti viene segnalato lo scarso utilizzo di cisplatino. Sempre facendo riferimento al periodo in esame, 12 dei 28 pazienti con carcinoma metastatico HER2+ sono stati trattati con una combinazione di derivati del platino, fluoropirimidine e trastuzumab, mentre i restanti erano inseriti in trial clinici che testavano nuovi farmaci anti-HER2 o analoghi.
Dei 76 pazienti HER2-, 37 sono stati trattati con una combinazione di oxaliplatino e fluoropirimidine (CAPOX), 32 con una combinazione di oxaliplatino e fluoruracile (FOLFOX), 3 con fluoropirimidine in monoterapia e 4 sono stati inseriti in trial clinici e sottoposti a immunoterapia.
In generale, la sospensione della chemioterapia per effetti collaterali avviene in una percentuale inferiore al 5% dei pazienti, mentre si assiste con maggiore frequenza (circa il 15% dei casi) a un depotenziamento (riduzione in termini di dosaggio) della terapia in relazione alle condizioni cliniche del paziente.
Rispetto ai criteri che guidano la scelta del trattamento si sottolinea che nella valutazione e caratterizzazione molecolare sono considerati in particolare mismatch repair, PD-L1 (mediante combined positive score – CPS) ed espressione di HER2.
Validazione della metodologia
Nel focus group è emersa la percezione, condivisa da tutti i partecipanti, di un aumento, negli ultimi anni, dei casi di tumore gastrico a esordio in età giovanile.
Nell’esperienza degli esperti, il tempo di progressione da carcinoma localmente avanzato a metastatico risulta pari a un anno in una percentuale di pazienti superiore al 40% (media 60%) raggiungendo circa il 90% entro i due anni. Questi valori risultano coerenti con quanto emerso dall’analisi real-world (Tabella V), nella quale la mediana è pari a 283 giorni (poco più di 9 mesi) e il 75% dei pazienti progredisce verso la malattia metastatica entro 584 giorni (più di un anno e mezzo).
Discussione
Il presente studio nasce in risposta a due esigenze principali: la carenza di evidenze recenti nella letteratura scientifica italiana circa i costi della gestione dei pazienti affetti da carcinoma gastrico e l’elevato grado di incertezza che ancora caratterizza i dati epidemiologici disponibili a livello nazionale. Nonostante l’evidente burden clinico ed economico della malattia, le fonti informative esistenti risultano frammentate e datate, caratteristica – questa – che mina l’affidabilità dei dati, in relazione in particolare alle nuove opzioni terapeutiche che si sono rese disponibili in anni recenti.
In questo contesto, lo studio è caratterizzato da un’impostazione metodologica mista, che combina dati amministrativi nazionali (flusso SDO), informazioni di dettaglio regionale (ASL Umbria 2) e validazione tramite expert opinion. Tale approccio consente non solo di sistematizzare l’informazione disponibile, ma anche di proporre una prima stima articolata e contestualizzata della prevalenza, dell’incidenza e dei costi del carcinoma gastrico in Italia, ponendo le basi per lo sviluppo di indicatori futuri e strategie più razionali di allocazione delle risorse.
L’analisi nazionale trasversale è risultata affidabile nel periodo 2015-2018, periodo nel quale l’incidenza rilevata corrisponde sostanzialmente a quella riportata ne “I numeri del cancro”, a conferma della solidità metodologica dello studio e dell’affidabilità dei dati nazionali quando opportunamente interpretati. Il numero di pazienti incidenti è risultato pari a 14.000 nel 2015 e subisce una graduale riduzione negli anni, fino ad arrivare a poco meno di 13.000 nel 2018 nell’intera penisola. La tendenza che negli ultimi anni si stia assistendo a una maggiore incidenza di casi con esordio in età giovanile, emerso nel focus group, appare in accordo con quanto riportato in letteratura [6,22].
Per quanto riguarda i pazienti con carcinoma gastrico localmente avanzato o metastatico, le stime di prevalenza negli anni centrali si aggirano tra 7.000 e 8.000 pazienti, con un’incidenza tendente alla diminuzione da 5.800 a 4.800. Anche la mortalità tende a ridursi.
L’impatto del carcinoma avanzato è rilevante non solo dal punto di vista dei costi e della sostenibilità del sistema, ma anche delle aspettative di cura. Tale evidenza rafforza l’importanza della prevenzione primaria e di strategie sanitarie mirate a intercettare precocemente i pazienti.
La discordanza con l’incidenza riportata ne “I numeri del cancro” per l’anno 2019 e per l’incidenza del sottogruppo localmente avanzato-metastatico, secondo l’opinione degli esperti, potrebbe dipendere dal cambio di percorso dei pazienti: negli ultimi anni un numero crescente di pazienti riceve diagnosi in ambulatorio, diagnosi che non è quindi riportata nel dato SDO. Tuttavia, in un secondo momento dovrebbe essere comunque possibile rilevare la registrazione dei ricoveri per gastrectomia.
La significativa variabilità regionale di incidenza rilevata nell’analisi delle SDO, con valori tendenzialmente più alti nelle regioni centrali, è stata ricondotta dagli esperti a differenze nei modelli organizzativi e nell’eventuale presenza di percorsi dedicati. Per esempio, nelle Marche si rileva una maggiore frequenza di ricoveri legata all’assenza di percorsi dedicati, che sono invece presenti in altre regioni, come la Lombardia, che ha fatto registrare un numero minore di ricoveri.
Un ulteriore fattore che contribuisce a spiegare l’eterogeneità osservata riguarda il diverso setting di gestione dei pazienti. Poiché l’analisi si basa esclusivamente sulle SDO, non vengono tracciati i pazienti seguiti in regime ambulatoriale. Ne deriva che, nelle regioni in cui prevale la gestione ambulatoriale, i dati potrebbero sottostimare la reale numerosità dei pazienti.
Nelle Marche, per esempio, la maggior parte dei casi viene gestita in ospedale, con conseguente incremento dei ricoveri rilevati. Al contrario, dove il modello organizzativo privilegia l’ambulatorio, la quota di ricoveri risulta più bassa, ma non necessariamente rappresenta un minore impatto complessivo della patologia.
L’analisi trasversale relativa alla regione Umbria è in linea con l’analisi nazionale per la prevalenza, mentre riporta tassi di mortalità maggiori perché tiene conto anche della mortalità extraospedaliera. In tutti gli anni l’incidenza dei pazienti con carcinoma gastrico localizzato è più alta rispetto a quella del localmente avanzato e del metastatico.
L’analisi longitudinale nazionale ha consentito di valutare l’evoluzione della patologia in un arco temporale di 5-9 anni, rilevando che è presente progressione di malattia nel 17,9% dei pazienti, con tempi di progressione piuttosto variabili.
I risultati dell’analisi condotta nella ASL Umbria 2, seppur su un campione limitato, offrono un’utile prima stima dei costi a carico del SSN: €12.797 per i pazienti con malattia localizzata, €18.505 per quelli con malattia localmente avanzata e €15.173 per i pazienti con carcinoma metastatico. La spesa è dominata dai costi ospedalieri, che rappresentano l’88% della spesa per i pazienti con carcinoma localizzato e carcinoma metastatico e il 91% per i pazienti con carcinoma localmente avanzato, ma è bene puntualizzare che, per la natura del dato, non è stato possibile considerare i farmaci infusivi somministrati in regime ospedaliero o ambulatoriale.
Uno studio risalente al 2018 [23] ha evidenziato che, sebbene il carcinoma gastrico costituisca di fatto un burden clinico e finanziario maggiore, sono disponibili solo pochi studi di costo-efficacia e sul costo di malattia, prevalentemente condotti in Asia, dai quali emergeva che il costo della gestione del carcinoma gastrico per paziente è generalmente più elevato rispetto a quello di molti altri tumori.
Un report stilato dall’Institute for Health Economics (IHE) svedese e pubblicato nel 2020 [24] ha calcolato che in Europa nel 2018 (sono stati inclusi 31 Paesi) il costo totale per il tumore allo stomaco era di circa 5 miliardi di euro, che rappresentavano il 3% dei costi sostenuti per i tumori.
In Italia nel 2018 i costi totali per i pazienti affetti dal tumore allo stomaco erano di 606,7 milioni di euro. In particolare, i costi diretti ammontavano a circa 180 milioni di euro, di cui più di 28 milioni dovuti al costo dei farmaci, i costi per le cure informali erano di circa 170 milioni di euro, i costi indiretti attribuibili alla mortalità erano più di 250 milioni di euro e quelli attribuibili alla morbilità eccedevano i 5 milioni di euro [24].
Non siamo a conoscenza di studi farmacoeconomici più recenti relativi alla realtà italiana.
Va considerato che tali stime si riferiscono a un periodo precedente all’introduzione su larga scala di nuovi trattamenti ad alto costo per la malattia metastatica. Si prevede dunque che i costi siano oggi ancora più elevati, alla luce dei cambiamenti nelle strategie terapeutiche, che comprendono anche l’impiego di farmaci target e immunoterapie.
Secondo le più recenti linee guida dell’European Society For Medical Oncology (ESMO) [25], la chirurgia (gastrectomia totale/subtotale con linfoadenectomia) è la principale opzione a intento curativo per malattia locale o locoregionale, alla quale, a seconda dello stadio, può essere abbinata la chemioterapia nel periodo perioperatorio.
Il carcinoma gastrico localmente avanzato/metastatico viene trattato mediante chemioterapia, con l’eventuale aggiunta di immunoterapia o di trastuzumab a seconda dell’espressione rispettivamente di PD-L1 e HER2 [25]. Quest’ultimo risulta espresso in circa il 20% delle neoplasie gastriche [1].
Per il tumore della giunzione gastro-esofagea locale o locoregionale, come riportato nelle relative linee guida ESMO [26], se di tipo adenocarcinoma, la terapia consiste in chemioterapia o chemioradioterapia, resezione chirurgica e chemioterapia o immunoterapia adiuvante.
Il tumore della giunzione gastro-esofagea di tipo adenocarcinoma avanzato viene trattato come il tumore gastrico [26].
Questo studio presenta alcuni limiti metodologici che ci permettono di fare alcune considerazioni: innanzitutto le SDO non nascono per finalità epidemiologiche o economiche e hanno evidenziato limiti ben noti, come l’incompletezza del dato sui decessi (non rilevando i decessi extraospedalieri), che giustifica l’introduzione del concetto di “persi al follow-up” per poter circoscrivere in maniera più accurata la stima della prevalenza. Inoltre, il riconoscimento della progressione da tumore localizzato a tumore localmente avanzato o metastatico potrebbe avvenire in ambulatorio e quindi non essere opportunamente tracciato dalle SDO oppure essere tracciato in un secondo momento; questo porta a una sottostima sistematica del numero di pazienti con tumore localmente avanzato o metastatico. Tuttavia, la loro elevata numerosità e la copertura nazionale rendono le SDO uno strumento utile se affiancato ad altre fonti. Si rileva, in ogni caso, la necessità di implementare il recupero delle informazioni mancanti nell’ottica di poter impostare eventuali indicatori di qualità delle strutture oncologiche nella gestione del paziente. Un’ulteriore criticità riguarda la classificazione dello stadio basata sui codici ICD9CM, che può determinare fenomeni di misclassificazione, ad esempio per diagnosi incomplete, codifiche non aggiornate o metastasi non registrate. Ciò può contribuire ulteriormente alla sottostima dei pazienti in stadio localmente avanzato o metastatico. Infine, il ricorso all’expert opinion, seppur motivato dalla scarsità di dati consolidati, introduce inevitabilmente elementi di soggettività. Tuttavia, tale approccio è spesso imprescindibile nella definizione di scenari real-world in aree a bassa evidenza. Dal punto di vista economico, la stima dei costi è stata condotta su una sola ASL (Umbria 2) e dunque rappresenta un dato preliminare, che necessiterebbe di validazione su scala più ampia. Un’ulteriore limitazione consiste nel fatto che le valorizzazioni economiche sono state effettuate utilizzando le tariffe regionali ospedaliere e ambulatoriali vigenti nel periodo di analisi (2014–2018) [27], e non tengono conto dell’aggiornamento più recente per le tariffe ambulatoriali [28]. Tuttavia, l’impatto di questa mancata rivalutazione risulta limitato, poiché la spesa ambulatoriale rappresenta nel nostro studio solo il 6% circa del costo totale annuo per paziente, a fronte di una quota pari all’88-91% attribuibile alle ospedalizzazioni (Tabella VI). Inoltre, il fatto che siano stati esclusi dall’analisi i costi relativi ai farmaci somministrati in regime ospedaliero o ambulatoriale non registrati a livello individuale nei sistemi informativi regionali potrebbe comportare una sottostima dei costi reali di trattamento. È opportuno precisare, tuttavia, che il periodo di osservazione (2014–2018) precede l’introduzione e la diffusione delle terapie oncologiche ad alto costo oggi disponibili, come gli inibitori dei checkpoint immunitari nivolumab e pembrolizumab. Pertanto, l’impatto economico di tale omissione risulta più contenuto nel periodo considerato di quanto non sarebbe nello scenario terapeutico attuale, in cui una quota crescente della spesa si concentra proprio sulla farmaceutica ospedaliera. Infine, per la natura puramente descrittiva dello studio, non sono stati fatti aggiustamenti dei costi dovuti all’inflazione.
Conclusioni
Il presente studio fornisce una fotografia aggiornata e articolata dell’epidemiologia e dell’impatto economico del carcinoma gastrico e della giunzione gastroesofagea in Italia, attraverso l’integrazione di dati amministrativi nazionali e regionali e il contributo dell’expertise clinica. I risultati ottenuti evidenziano una riduzione dei tassi di incidenza, un picco nella prevalenza nell’anno 2017 e una significativa variabilità regionale nella gestione ospedaliera della patologia.
Dal punto di vista economico, lo studio ha stimato costi annuali rilevanti per paziente, dominati dalle ospedalizzazioni. Tali stime, sebbene preliminari e riferite a un’epoca pre-immunoterapia diffusa, suggeriscono che l’onere economico del carcinoma gastrico sia destinato ad aumentare nei prossimi anni, rendendo urgente una pianificazione più efficiente delle risorse.
I limiti insiti nelle fonti utilizzate sottolineano la necessità di sviluppare sistemi informativi integrati e aggiornati, capaci di fornire dati più accurati. In un’ottica di sanità pubblica, emerge con forza l’importanza di potenziare le strategie di prevenzione e diagnosi precoce, con l’obiettivo di migliorare la sopravvivenza e ridurre il burden economico della malattia.
Conflicts of interest
M.D.B. has received grants or contracts from LILLY SpA, AMGEN, and BMS.
P.D.R. is an employee of Astellas Pharma Italia.
A.M. has received consulting fees and payment or honoraria for lectures, presentations, speakers’ bureaus, manuscript writing or educational events from Abbott, BMS, MSD, ROCHE, Sanofi, J&J, and others.
P.S., A.R., R.B., E.M., F.B. have no conflicts of interest to declare other than funding of this project and medical writing assistance.
Funding
This work was funded by Astellas Pharma Italia. Medical writing support, conducted in accordance with Good Publication Practice (GPP 2022) and the International Committee of Medical Journal Editors (ICMJE) guidelines, was funded by Astellas Pharma Italia.
Bibliografia
1.AIOM, AIRTUM, Fondazione AIOM. I numeri del cancro in Italia 2022. https://www.aiom.it/wp-content/uploads/2022/12/2022_AIOM_NDC-web.pdf. Accessed April 4, 2025
2.World Health Organization. Stomach fact sheet. https://gco.iarc.who.int/media/globocan/factsheets/cancers/7-stomach-fact-sheet.pdf. Accessed July 9, 2025
3.AIOM, AIRTUM, Fondazione AIOM. I numeri del cancro in Italia 2025. https://www.aiom.it/wp-content/uploads/2025/12/2025_NDC_web.pdf. Accessed September 12, 2025
4.Morgan E, Arnold M, Camargo MC, et al. The current and future incidence and mortality of gastric cancer in 185 countries, 2020–40: A population-based modelling study. eClinicalMedicine 2022; 47: 101404; https://doi.org/10.1016/j.eclinm.2022.101404
5.Arnold M, Park JY, Camargo MC, et al. Is gastric cancer becoming a rare disease? A global assessment of predicted incidence trends to 2035. Gut 2020; 69: 823-29; https://doi.org/10.1136/gutjnl-2019-320234
6.Ferlay J, Colombet M, Soerjomataram I, et al. Cancer statistics for the year 2020: An overview. International Journal of Cancer 2021; 149: 778-89; https://doi.org/10.1002/ijc.33588
7.Hooi JKY, Lai WY, Ng WK, et al. Global Prevalence of Helicobacter pylori Infection: Systematic Review and Meta-Analysis. Gastroenterology 2017; 153: 420-29; https://doi.org/10.1053/j.gastro.2017.04.022
8.Ayers B, Forshaw M, Hunter MS. The impact of attitudes towards the menopause on women’s symptom experience: a systematic review. Maturitas 2010; 65: 28-36; https://doi.org/10.1016/j.maturitas.2009.10.016
9.AIOM, AIRTUM, Fondazione AIOM. I numeri del cancro in Italia 2011. http://media.aiom.it/userfiles/files/doc/documenti_scientifici/2011_Numeri_del_cancro_AIOM_AIRTUM.pdf. Accessed July 3, 2025
10.AIOM, CCM, AIRTUM. I numeri del cancro in Italia 2012. http://media.aiom.it/userfiles/files/doc/documenti_scientifici/2012_Numeri_del_cancro_AIOM_AIRTUM.pdf. Accessed July 3, 2025
11.AIOM, CCM, AIRTUM. I numeri del cancro in Italia 2013. http://media.aiom.it/userfiles/files/doc/documenti_scientifici/2013_Numeri_del_cancro_AIOM_AIRTUM.pdf. Accessed July 3, 2025
12.AIOM, CCM, AIRTUM. I numeri del cancro in Italia 2014. http://media.aiom.it/userfiles/files/doc/documenti_scientifici/2014_Numeri_del_cancro_AIOM_AIRTUM.pdf. Published 2014. Accessed July 3, 2025
13.AIOM, CCM, AIRTUM. I numeri del cancro in Italia 2015. http://media.aiom.it/userfiles/files/doc/documenti_scientifici/2015_I_Numeri_del_cancro.pdf. Accessed July 3, 2025
14.AIOM, AIRTUM. I numeri del cancro in Italia 2016. http://media.aiom.it/userfiles/files/doc/documenti_scientifici/2016_numeri_del_cancro_AIOM-AIRTUM.pdf. Accessed July 3, 2025
15.AIOM, AIRTUM, Fondazione AIOM. I numeri del cancro in Italia 2017. http://media.aiom.it/userfiles/files/doc/documenti_scientifici/2017_numeri_del_cancro.pdf. Accessed July 3, 2025
16.AIOM, AIRTUM, Fondazione AIOM. I numeri del cancro in Italia 2018. https://www.aiom.it/wp-content/uploads/2018/10/2018_NumeriCancro-operatori.pdf. Accessed July 3, 2025
17.AIOM, AIRTUM, Fondazione AIOM. I numeri del cancro in Italia 2019. https://www.aiom.it/wp-content/uploads/2019/09/2019_Numeri_Cancro-operatori-web.pdf. Accessed July 3, 2025
18.Rothman KJ, Greenland S, Lash TL. Modern epidemiology. 3rd ed. Philadelphia: Wolters Kluwer health - Lippincott Williams & Wilkins; 2008
19.ISTAT. Popolazione residente. https://demo.istat.it/app/?i=POS&l=it. Accessed July 3, 2025
20.Regione Umbria. Tariffario regionale per le prestazioni ospedaliere, farmaceutiche e ambulatoriali. Regione Umbria. https://www.regione.umbria.it/salute. Published 2018. Accessed July 3, 2025
21.Farmadati Italia srl. GALLERY® - Compendio Farmaceutico WEB - ©Farmadati Italia. https://gallery.farmadati.it/. Accessed July 3, 2025
22.Anderson WF, Rabkin CS, Turner N, et al. The Changing Face of Noncardia Gastric Cancer Incidence Among US Non-Hispanic Whites. JNCI: Journal of the National Cancer Institute 2018; 110: 608-15; https://doi.org/10.1093/jnci/djx262
23.Casamayor M, Morlock R, Maeda H, et al. Targeted literature review of the global burden of gastric cancer. Ecancermedicalscience 2018; 12: 883; https://doi.org/10.3332/ecancer.2018.883
24.Hofmarcher T, Lindgren P. The cost of cancers of the digestive system in Europe. IHE Report. 2020
25.Lordick F, Carneiro F, Cascinu S, et al. Gastric cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Annals of Oncology 2022; 33: 1005-20; https://doi.org/10.1016/j.annonc.2022.07.004
26.Obermannová R, Alsina M, Cervantes A, et al. Oesophageal cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Annals of Oncology 2022; 33: 992-1004; https://doi.org/10.1016/j.annonc.2022.07.003
27.Ministero della Salute. DECRETO 18 ottobre 2012 Remunerazione prestazioni di assistenza ospedaliera per acuti, assistenza ospedaliera di riabilitazione e di lungodegenza post acuzie e di assistenza specialistica ambulatoriale. (13A00528) (GU Serie Generale n.23 del 28-01-2013 - Suppl. Ordinario n. 8). https://www.gazzettaufficiale.it/eli/id/2013/01/28/13A00528/sg. Published 2012. Accessed December 10, 2025
28.Ministero della Salute. DECRETO 25 novembre 2024 Definizione delle tariffe relative all’assistenza specialistica ambulatoriale e protesica. (24A06929) (GU Serie Generale n.302 del 27-12-2024). https://www.gazzettaufficiale.it/eli/id/2024/12/27/24A06929/SG. Published 2024. Accessed December 10, 2025